Abstrakt
ChromatografickĂ© techniky spoÄĂvajĂ v rĆŻznĂœch
fyzikĂĄlnÄ-chemickĂœch principech dÄlenĂ smÄsi lĂĄtek na jednotlivĂ© sloĆŸky.
Mechanismus chromatografickĂ©ho dÄlenĂ vyuĆŸĂvĂĄ zadrĆŸenĂ (retenci) smÄsi stacionĂĄrnĂ
fĂĄzĂ a postupnĂ© a opakovanĂ© vytvĂĄĆenĂ rovnovĂĄĆŸnĂœch stavĆŻ dÄlenĂœch lĂĄtek mezi
pĆĂtomnĂœmi fĂĄzemi.
SouvisejĂcĂ informace
Text
ZĂĄkladnĂ informace o chromatografickĂœch technikĂĄch jsou
rozdÄleny podle schĂ©matu:
1.
Chromatografické
metody - Ășvod, pĆehled
2.
Faktory
ovlivĆujĂcĂ chromatografickĂ© dÄlenĂ
A. Termodynamické faktory
separace
B. Kinetické faktory separace
3.
ZĂĄklady
hodnocenĂ chromatografickĂœch dat
4.
PĆĂprava
vzorkĆŻ
5.
Derivatizace
1.
ChromatografickĂ© metody - Ășvod, pĆehled
PrincipiĂĄlnĂ zĂĄklad vĆĄem chromatografickĂœm technikĂĄm
poloĆŸil na poÄĂĄtku dvacĂĄtĂ©ho stoletĂ M.S. Cvet (1872 - 1919), ruskĂœ botanik,
fyziolog a biochemik, kdyĆŸ rozdÄlil na sloupci sorbentu listovĂĄ barviva.
PĆehled chromatografickĂœch
metod
|
MobilnĂ fĂĄze |
StacionĂĄrnĂ fĂĄze |
Mechanismus dÄlenĂ |
Metoda |
|
plyn |
kapalina |
rozdÄlovĂĄnĂ, rozdÄlovacĂ, |
plynovĂĄ rozdÄlovacĂ |
|
|
|
rovnovĂĄha |
chromatografie (GLC) |
|
|
pevnĂĄ
lĂĄtka |
adsorpce, adsorpÄnĂ |
plynovĂĄ adsorpÄnĂ |
|
|
|
izoterma |
chromatografie (GSC) |
|
|
|
sĂtovĂœ efekt |
plynovĂĄ chromatografie |
|
|
|
|
na molekulovĂœch sĂtech (GSC) |
|
kapalina |
kapalina |
rozdÄlovĂĄnĂ, rozdÄlovacĂ |
kapalinovĂĄ rozdÄlovacĂ |
|
|
|
rovnovĂĄha |
chromatografie (LLC) |
|
|
|
sĂtovĂœ efekt |
gelovĂĄ permeaÄnĂ |
|
|
|
|
chromatografie (GPC) |
|
|
pevnĂĄ
lĂĄtka |
adsorpce, adsorpÄnĂ |
kapalinovĂĄ chromatografie |
|
|
|
izoterma |
adsorpÄnĂ (LSC) |
|
|
|
|
tenkovrstvĂĄ |
|
|
|
|
chromatografie (TLC) |
|
|
|
iontovĂĄ vĂœmÄna, |
ionexovĂĄ chromatografie |
|
|
|
vĂœmÄnnĂĄ rovnovĂĄha |
(IEC) |
|
|
|
biospecifickĂĄ chemickĂĄ |
afinitnĂ |
|
|
|
chemickĂĄ reakce |
chromatografie |
StacionĂĄrnĂ (nepohyblivĂĄ) fĂĄze - je umĂstÄna v kolonÄ
(vrstvÄ), mĆŻĆŸe bĂœt pĆedstavovĂĄna ÄĂĄsteÄkami pevnĂ© hmoty ( stacionĂĄrnĂ fĂĄze v kapalinovĂ© chromatografii ) nebo kapalinou zakotvenou na povrchu inertnĂho
nosiÄe.
MobilnĂ (pohyblivĂĄ) fĂĄze - (plyn, kapalina) unĂĄĆĄĂ
separovanĂ© sloĆŸky loĆŸem stacionĂĄrnĂ fĂĄze.
2. Faktory ovlivĆujĂcĂ chromatografickĂ© dÄlenĂ
Termodynamické faktory separace
Termodynamické faktory separace
zahrnujĂ vliv interakce chromatografovanĂœch sloĆŸek se sorbentem a z toho
vyplĂœvajĂcĂ i rozdĂlnĂ© mechanismy separace. HlavnĂmi principy
chromatografickĂ©ho dÄlenĂ jsou adsorpce, rozdÄlovĂĄnĂ mezi dvÄ fĂĄze, chemisorpce
a sĂtovĂœ efekt.
(a)
Adsorpce na polĂĄrnĂch adsorbentech a chemisorpce
PĆi adsorpci molekul na tuhĂœch
adsorbentech dochĂĄzĂ k jejich zachycovĂĄnĂ na povrchu tuhĂ© fĂĄze. JestliĆŸe
pronikajĂ pĆes rozhranĂ tuhĂ© fĂĄze a difundujĂ do jejĂho objemu, jednĂĄ se o
adsorpci. RozhodujĂcĂ vĂœznam pĆi adsorpci mĂĄ velikost a jakost povrchu
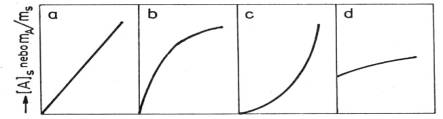
adsorbentu, kde se nachĂĄzĂ tzv. adsorpÄnĂ centra. ZĂĄvislost adsorbovanĂ©ho
mnoĆŸstvĂ lĂĄtky na koncentraci tĂ©ĆŸe lĂĄtky v okolnĂm prostĆedĂ udĂĄvĂĄ adsorpÄnĂ
izoterma. V reĂĄlnĂœch systĂ©mech se uplatĆujĂ dvÄ izotermy, a to Langmuirova a
Freundlichova.
|
|
|
|
(b)
RozdÄlovĂĄnĂ mezi dvÄ nemĂsitelnĂ© fĂĄze
Tento mechanismus pĆevlĂĄdĂĄ v
plynovĂ© chromatografii. Dostanou-li se do styku dvÄ nemĂsitelnĂ© fĂĄze (obÄ
kapalnĂ©, nebo kapalnĂĄ a plynnĂĄ) z nichĆŸ jedna obsahuje urÄitou sloĆŸku (smÄs
lĂĄtek) a druhĂĄ nikoli, difunduje tato do ÄistĂ© fĂĄze tak, aby byl zachovĂĄn urÄitĂœ
pomÄr, kterĂœ je za danĂœch podmĂnek konstantnĂ. HnacĂ silou tohoto partiÄnĂho
procesu je rozdĂl koncentracĂ sloĆŸky v jednĂ© a druhĂ© fĂĄzi, protoĆŸe systĂ©m mĂĄ
snahu dostat se do rovnovĂĄhy.
(c)
SĂtovĂœ efekt
Na principu sĂtovĂ©ho efektu
jsou zaloĆŸeny dvÄ techniky. V plynnĂ© fĂĄzi je to chromatografie na molekulĂĄrnĂch
sĂtech vyuĆŸĂvajĂcĂ rozdĂlnĂœch, pĆesnÄ definovanĂœch pĂłrĆŻ sorbentu k separaci
plynĆŻ podle velikosti prĆŻmÄru jejich molekul Äi atomĆŻ. V kapalnĂ© fĂĄzi jde
o gelovou permeaÄnĂ chromatografii .
(d)
VzĂĄjemnĂĄ interakce molekul
Sorpce lĂĄtek je podmĂnÄna
silami, jimiĆŸ na sebe pĆŻsobĂ navzĂĄjem sorbent a sorbovanĂĄ lĂĄtka. JednĂĄ se o
sĂly nepolĂĄrnĂ (van der Waalsovy) a polĂĄrnĂ (indukovanĂ©, disperznĂ, vazebnĂ©),
kterĂ© se mohou uplatĆovat (interakce vzorek - vzorek, vzorek - sorbent, vzorek
- mobilnĂ fĂĄze).
Kinetické faktory separace
KinetickĂ© faktory zahrnujĂ
vlivy rychlosti prĆŻtoku mobilnĂ fĂĄze, difĂșze sloĆŸek v mobilnĂ i stacionĂĄrnĂ
fĂĄzi atd. na rozĆĄiĆovĂĄnĂ eluÄnĂch kĆivek. K vystiĆŸenĂ tÄchto vlivĆŻ se zavĂĄdÄjĂ
pojmy teoretickĂ© patro, kapacitnĂ pomÄr, ĂșÄinnost a dalĆĄĂ. MĂra relativnĂ
separace dvou lĂĄtek se nazĂœvĂĄ rozliĆĄenĂ. RozliĆĄenĂ je zĂĄvislĂ© na vztahu mezi
selektivitou, kapacitou a ĂșÄinnostĂ.
(a)
Teoretické patro
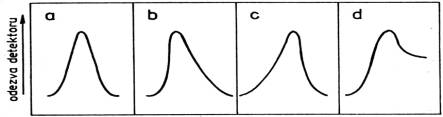
TeoretickĂ© patro je mĂrou ĂșÄinnosti
chromatografickĂ©ho systĂ©mu, bezprostĆednÄ s nĂ souvisĂ tvar eluÄnĂ kĆivky.
Vlivy difĂșze bÄhem chromatografickĂœch pochodĆŻ se projevujĂ rozĆĄiĆovĂĄnĂm eluÄnĂ
kĆivky. Je-li znĂĄma celkovĂĄ dĂ©lka kolony (L), je moĆŸno vypoÄĂtat vĂœĆĄku (H)
ekvivalentnĂ teoretickĂ©mu patru, na jejĂmĆŸ zĂĄkladÄ se porovnĂĄvajĂ ĂșÄinnosti
jednotlivĂœch chromatografickĂœch kolon.
(b)
DifĂșznĂ teorie
Tato teorie respektuje
neideĂĄlnĂ chovĂĄnĂ sloĆŸek v chromatografickĂ© kolonÄ a pĆipisuje projevy tohoto
chovĂĄnĂ tĆem hlavnĂm vlivĆŻm: turbulentnĂ difĂșzi v mobilnĂ fĂĄzi (HT),
molekulĂĄrnĂ difĂșzi v mobilnĂ fĂĄzi (HM) a odporu vĆŻÄi pĆevodu hmoty
na fĂĄzovĂ©m rozhranĂ (HO). Tyto vlivy jsou nezĂĄvislĂ© a podĂlĂ se na
vĂœĆĄce ekvivalentnĂ teoretickĂ©mu patru:
H = HT + HM
+ HO
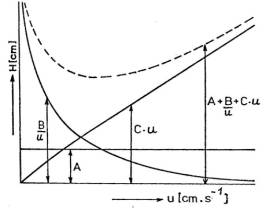
Souvislost mezi difĂșznĂmi vlivy
a lineĂĄrnĂ rychlostĂ mobilnĂ fĂĄze odvodil van Deemter. V nejjednoduĆĄĆĄĂm tvaru
mĂĄ van Deemterova rovnice tvar:
H = A + B/u + C * u
|
|
kde: A - faktor vlivu turbulentnĂ difĂșze, B - faktor vlivu molekulĂĄrnĂ difĂșze, C - faktor vlivu odporu vĆŻÄi pĆevodu hmoty, u - stĆednĂ lineĂĄrnĂ rychlost toku mobilnĂ fĂĄze. |
(c)
RozliĆĄenĂ
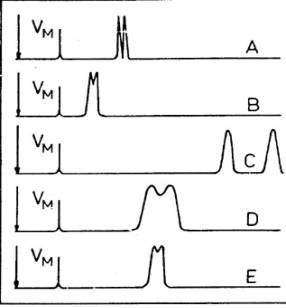
CĂlem chromatografie je
dosĂĄhnout dobrĂ©ho rozdÄlenĂ analyzovanĂœch lĂĄtek v pĆijatelnĂ©m Äase. RozdÄlenĂ
mĆŻĆŸe bĂœt ĂșplnĂ©, ÄĂĄsteÄnĂ©, nedokonalĂ©. KvantitativnÄ je zavedena mĂra relativnĂ
separace dvou lĂĄtek a nazĂœvĂĄ se rozliĆĄenĂ R1,2.
Z praktickĂ©ho hlediska je tĆeba
vÄdÄt, jak lze rozliĆĄenĂ mÄnit, kterĂ© faktory a jak hodnotu rozliĆĄenĂ
ovlivĆujĂ:
R1,2 = Fselektivity
* Fkapacity * FĂșÄinnosti
Faktor selektivity
Selektivita systému danå volbou
stacionĂĄrnĂ a mobilnĂ fĂĄze hraje v chromatografii rozhodujĂcĂ Ășlohu. Separace
sloĆŸek u instrumentĂĄlnÄ nejjednoduĆĄĆĄĂch technik jako jsou papĂrovĂĄ a
tenkovrstvĂĄ chromatografie je zaloĆŸena pouze na selektivitÄ systĂ©mu. SelektivnĂ
faktor je faktorem termodynamickĂœm a je nÄkdy vyjadĆovĂĄn pomocĂ separaÄnĂho
faktoru a, kterĂœ je roven pomÄru distribuÄnĂch konstant.
Lze odvodit, ĆŸe rozliĆĄenĂ je ĂșmÄrnĂ© vĂœrazu (1 - a).
Hodnotu rozliĆĄenĂ je moĆŸno
ovlivnit:
-
zmÄnou
stacionĂĄrnĂ fĂĄze,
-
zmÄnou
mobilnĂ fĂĄze,
-
souÄasnou
zmÄnou obou fĂĄzĂ,
-
zmÄnou
rychlosti toku mobilnĂ fĂĄze.
|
|
Faktor kapacity
KapacitnĂ pomÄr k je
bezrozmÄrnĂĄ veliÄina udĂĄvajĂcĂ hodnotu retence separovanĂ© sloĆŸky:
k = KD
* Vs/Vm
kde: KD - distribuÄnĂ
konstanta, Vs a Vm jsou objemy stacionĂĄrnĂ a mobilnĂ
fĂĄze.
Hodnota rozliĆĄenĂ roste se
vzrĆŻstajĂcĂ hodnotou kapacitnĂho pomÄru. KapacitnĂ pomÄr lze ovlivnit:
-
mnoĆŸstvĂm
stacionĂĄrnĂ fĂĄze v kolonÄ,
-
zmÄnou
stacionĂĄrnĂ nebo mobilnĂ fĂĄze (v HPLC gradientovou elucĂ),
-
zmÄnou
teploty kolony (v GC stupĆovitĂĄ i gradientovĂĄ).
-
Faktor ĂșÄinnosti
Faktor ĂșÄinnosti je faktorem
kinetickĂœm a ukazuje, ĆŸe rozliĆĄenĂ je ĂșmÄrnĂ© druhĂ© odmocninÄ celkovĂ©ho poÄtu
pater kolony. Faktor ĂșÄinnosti lze ovlivnit:
-
délkou
kolony,
-
rychlostĂ
prĆŻtoku mobilnĂ fĂĄze,
-
velikostĂ
ÄĂĄstic sorbentu,
-
teplotou,
viskozitou mobilnĂ i stacionĂĄrnĂ fĂĄze apod.
3. ZĂĄklady hodnocenĂ chromatografickĂœch dat
VyjadĆovĂĄnĂ vĂœsledkĆŻ ve vĆĄech kolonovĂœch
chromatografickĂœch technikĂĄch je shodnĂ©. Po nĂĄstĆiku vzorku do chromatografickĂ©
kolony je unĂĄĆĄen eluÄnĂ pĂĄs (smÄsnĂĄ zĂłna) mobilnĂ fĂĄzĂ a na kolonÄ naplnÄnĂ©
sorbentem dochĂĄzĂ k jejich separaci (rozdÄlenĂ). PĆi vĂœstupu sloĆŸky smÄsi z
kolony indikuje detektor jejĂ pĆĂtomnost v eluĂĄtu a zaznamenĂĄvĂĄ graficky eluÄnĂ
pĂk (kĆivku). Poloha pĂku udĂĄvĂĄ dobu, kterou separovanĂĄ sloĆŸka setrvĂĄ v kolonÄ,
tj. eluÄnĂ (retenÄnĂ) Äas a je kvalitativnĂm prĆŻkazem pĆĂtomnosti danĂ© sloĆŸky.
Plocha (vĂœĆĄka) pĂku se kvantifikuje a udĂĄvĂĄ mnoĆŸstvĂ sloĆŸky obsaĆŸenĂ© v
separovanĂ© smÄsi.
PĆi kvantitativnĂ analĂœze je tĆeba ĆeĆĄit vztah mezi
plochou (vĂœĆĄkou) pĂku a mnoĆŸstvĂm sloĆŸky ve vzorku a zĂskanĂ© vĂœsledky hodnotit
z hlediska pĆesnosti a sprĂĄvnosti. Pro urÄenĂ obsahu sloĆŸky analyzovanĂ©ho
vzorku se pouĆŸĂvĂĄ:
a.
Metoda
absolutnĂ kalibrace (metoda vnÄjĆĄĂho standardu) spoÄĂvĂĄ v dĂĄvkovĂĄnĂ znĂĄmĂœch
mnoĆŸstvĂ analyzovanĂ©ho vzorku a standardu za identickĂœch podmĂnek a to buÄ
metodou kalibraÄnĂ kĆivky nebo metodou pĆĂmĂ©ho srovnĂĄnĂ.
b.
Metoda
vnitĆnĂho standardu je zaloĆŸena na pĆidĂĄnĂ znĂĄmĂ©ho mnoĆŸstvĂ jednĂ© lĂĄtky, kterĂĄ
neinterferuje s ostatnĂmi sloĆŸkami smÄsi. Tato metoda eliminuje pĆĂpadnĂ©
nepĆesnosti v dĂĄvkovĂĄnĂ vzorku nebo ztrĂĄty pĆi pĆedĂșpravÄ vzorku.
c.
Metoda
standardnĂho pĆĂdavku vyuĆŸĂvĂĄ pĆidĂĄnĂ definovanĂ©ho mnoĆŸstvĂ standardu ke
znĂĄmĂ©mu mnoĆŸstvĂ vzorku.
4. PĆĂprava vzorkĆŻ
KromÄ vlastnĂho analytickĂ©ho zpracovĂĄnĂ vzorkĆŻ jsou
vĂœsledky analĂœz znaÄnÄ ovlivnÄny i zpĆŻsobem odbÄru a dalĆĄĂm zpracovĂĄnĂm vzorkĆŻ
pĆed analĂœzou.
ObohacovacĂ techniky a Ășprava vzorkĆŻ
DĆŻvody pro pouĆŸitĂ:
-
na
chromatografickou kolonu nelze pĆĂmo dĂĄvkovat biologickĂœ materiĂĄl,
-
koncentrace
stanovované låtky je pod limitem detekce,
-
stanovovanĂĄ
lĂĄtka je doprovĂĄzena jinĂœmi lĂĄtkami, kterĂ© ruĆĄĂ analĂœzu.
Techniky Ășpravy vzorkĆŻ:
1.
adsorpÄnĂ
2.
metody
vyuĆŸĂvajĂcĂ chemickĂ© reakce
3.
vymrazovacĂ
(kryogennĂ)
4.
odluÄovacĂ
(trapping)
5.
extrakÄnĂ
- plynem (headspace), pevnou lĂĄtkou (SPE), kapalinou (extrakce mezi
nemĂsitelnĂœmi kapalinami, destilaÄnĂ extrakÄnĂ technika)
6.
ultrafiltraÄnĂ
V klinickĂ© chemii se pouĆŸĂvajĂ hlavnÄ techniky extrakÄnĂ
a ultrafiltraÄnĂ, ostatnĂ zpĆŻsoby obohacovĂĄnĂ vzorkĆŻ se uplatĆujĂ pĆedevĆĄĂm v
technické praxi.
ExtrakÄnĂ techniky:
(a)
extrakce plynem
Pro postupy zahrnujĂcĂ obecnÄ
extrakci studovanĂ©ho materiĂĄlu plynem a nĂĄsledujĂcĂ plynovÄ chromatografickou
analĂœzu plynnĂ©ho extraktu se vĆŸil nĂĄzev headspace analĂœza. JednĂĄ se o postupy,
kterĂœmi se stanovujĂ obsahy tÄkavĂœch sloĆŸek kondenzovanĂœch materiĂĄlĆŻ analĂœzou
plynnĂ© fĂĄze, kterĂĄ je v kontaktu (zpravidla v rovnovĂĄze) s analyzovanĂœm
kondenzovanĂœm materiĂĄlem. V klinickĂ© praxi je pouĆŸitelnĂĄ tzv. statickĂĄ
headspace, kdy se analyzuje vzorek plynu odebranĂœ z prostoru nad kondenzovanou
fĂĄzĂ uzavĆenĂ©ho systĂ©mu, kterĂœ je s nĂ v rovnovĂĄze (napĆ. analĂœza tÄkavĂœch
lĂĄtek v krvi).
(b)
extrakce kapalinou
Extrakce mezi dvÄma
nemĂsitelnĂœmi kapalinami vyuĆŸĂvĂĄ zĂĄkonitostĂ Nernstova rozdÄlovacĂho zĂĄkona.
ZĂĄkladnĂ podmĂnkou je dobrĂĄ rozpustnost sledovanĂœch komponent v pouĆŸitĂ©m
rozpouĆĄtÄdle a takĂ© znalost velikosti distribuÄnĂch konstant v danĂ©m systĂ©mu.
OrganickĂœ extrakt se zpravidla odpaĆuje v proudu inertnĂho plynu (dusĂku) a
odparek se rozpustĂ pĆed aplikacĂ na chromatografickou kolonu v nezbytnĂ©m
objemu mobilnĂ fĂĄze.
(c)
extrakce pevnou lĂĄtkou (SPE)
Technika izolace, ÄiĆĄtÄnĂ nebo
obohacovĂĄnĂ stanovovanĂ© sloĆŸky na malĂœch kolonkĂĄch (napĆ. velikosti injekÄnĂ
stĆĂkaÄky) naplnÄnĂœch sorbentem, iontomÄniÄem, gelem nebo jinĂœm dÄlĂcĂm mĂ©diem
dle charakteru izolovanĂ© lĂĄtky. Vzorek v roztoku se prolĂ©vĂĄ nebo prosĂvĂĄ
podtlakem, zachycenĂ© sloĆŸky se po promytĂ uvolnĂ vhodnĂœm rozpouĆĄtÄdlem.
Pro SPE se Äasto vyuĆŸĂvĂĄ pĆedevĆĄĂm modifikovanĂ©ho silikagelu:
|
Typ sorbentu (vĂĄzanĂĄ funkÄnĂ skupina) |
Typ interakcĂ |
PĆĂklady aplikacĂ |
|
Silikagel O |
adsorpce polĂĄrnĂch lĂĄtek |
steroidy, lipidy, org.
kyseliny, |
|
|
l |
lĂ©Äiva |
|
oktadecyl- |
RP* extrakce nepolĂĄrnĂch a |
steroidy, nitraminy |
|
|
stĆednÄ polĂĄrnĂch lĂĄtek |
|
|
kyanopropyl- |
NP** extrakce polĂĄrnĂch lĂĄtek |
aminy, alkoholy, barviva, |
|
|
|
fenoly |
|
diol- |
NP extrakce polĂĄrnĂch lĂĄtek |
proteiny, peptidy |
|
aminopropyl- (dimethylaminopropyl-) |
extrakce na principu slabĂ© iontovĂ© vĂœmÄny |
peptidy, nukleotidy,
steroidy, vitamĂny, cukry, aminokyseliny |
|
aromatické sulfonové kyseliny |
extrakce na silnĂœch katexech
a RP extrakce (kromÄ mechanismu iontovĂœch pĂĄrĆŻ) |
aminokyseliny, katecholaminy,
nukleové båze, nukleosidy |
|
kvarternĂ aminy |
extrakce na silnĂœch anexech |
nukleosidy, nukleové
kyseliny, antibiotika |
** RP - systĂ©m obrĂĄcenĂœch fĂĄzĂ
** NP - systĂ©m normĂĄlnĂch fĂĄzĂ
(d)
Ultrafiltrace
Ultrafiltrace je metoda
obohacovĂĄnĂ nebo dÄlenĂ roztokĆŻ pomocĂ polopropustnĂœch membrĂĄn. Hustota
membråny limituje velikost molekul, které jsou separovåny. Tato technika je
vhodnĂĄ pro deproteinaci sĂ©rovĂœch vzorkĆŻ, provedenĂ je moĆŸnĂ© i v malĂœch objemech
vzorku (centrifugaÄnĂ filtrace ve zkumavkĂĄch typu Eppendorf).
5. Derivatizace
DerivatizaÄnĂ techniky vyuĆŸĂvajĂ specifickĂ© reakce pĆed,
v prĆŻbÄhu chromatografickĂ©ho procesu, nebo po jeho ukonÄenĂ pĆed vstupem do
detektoru. Smyslem je docĂlit kvalitativnÄ novĂœch vlastnostĂ separovanĂœch
lĂĄtek, kterĂ© umoĆŸnĂ pĆedseparaci Äi separaci vĆŻbec, usnadnĂ identifikaci, zvĂœĆĄĂ
citlivost vlastnĂ detekce. KaĆŸdĂĄ z chromatografickĂœch technik klade na
pĆipravenĂ© derivĂĄty jinĂ© poĆŸadavky. U plynovĂ© chromatografie je tĆeba docĂlit
toho, aby vznikajĂcĂ derivĂĄty byly tÄkavÄjĆĄĂ neĆŸ lĂĄtky pĆŻvodnĂ, zatĂmco v
kapalinovĂ© chromatografii v ploĆĄnĂ©m uspoĆĂĄdĂĄnĂ je tomu naopak. U kapalinovĂ©
kolonovĂ© chromatografie nehraje tenze par separovanĂœch sloĆŸek vĂœznamnou roli,
ale jde pĆedevĆĄĂm o vyvolĂĄnĂ zmÄn v rozpustnosti jednotlivĂœch komponent
obsaĆŸenĂœch ve smÄsi.
PoznĂĄmky
Appendixy
Literatura
Autorské poznåmky
Jaroslava VĂĄvrovĂĄ