Abstrakt
Pr┼»b─øh acidobazick├¢ch, sr├í┼¥ec├¡ch, komplexotvorn├¢ch a
oxida─ìn─ø reduk─ìn├¡ch titrac├¡ lze sledovat potenciometricky. Do titrovan├®ho
roztoku se ponoří vhodná indikační a referenční elektroda a zaznamenává se závislost
nap─øt├¡ na mno┼¥stv├¡ p┼Öid├ívan├®ho odm─ørn├®ho roztoku. Grafick├¢m zobrazen├¡m
z├ívislosti potenci├ílu nebo z├íporn├®ho logaritmu koncentrace stanovovan├®ho iontu
(pH, pX) na stupni titrace vznik├í titira─ìn├¡ k┼Öivka esovit├®ho tvaru. Hodnota
potenci├ílu v bod─ø ekvivalence je ur─ìov├ína velikost├¡ p┼Ö├¡slu┼ín├® rovnov├í┼¥n├®
konstanty podle typu titrace. Potenciometrick├í metoda umo┼¥┼êuje postupn├®
stanoven├¡ dvou i v├¡ce slo┼¥ek za p┼Öedpokladu, ┼¥e se jejich rovnov├í┼¥n├® konstanty
od sebe dostate─ìn─ø li┼í├¡.
Související informace
Text
Pr┼»b─øh acidobazick├¢ch, sr├í┼¥ec├¡ch, komplexotvorn├¢ch a
oxida─ìn─ø reduk─ìn├¡ch titrac├¡ lze sledovat potenciometricky. Do titrovan├®ho
roztoku se ponoří vhodná indikační a referenční elektroda a zaznamenává se
z├ívislost nap─øt├¡ na mno┼¥stv├¡ p┼Öid├ívan├®ho odm─ørn├®ho roztoku. Hodnota potenci├ílu
v bod─ø ekvivalence (Ekv) je ur─ìov├ína velikost├¡ p┼Ö├¡slu┼ín├® rovnov├í┼¥n├®
konstanty podle typu titrace. Potenciometrick├í metoda umo┼¥┼êuje postupn├®
stanoven├¡ dvou i v├¡ce slo┼¥ek za p┼Öedpokladu, ┼¥e se jejich rovnov├í┼¥n├® konstanty
od sebe dostate─ìn─ø li┼í├¡.
|
|
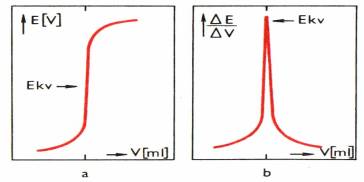
a)
Potenciometrická
k┼Öivka (z├ívislost nap─øt├¡ na objemu p┼Öid├ívan├®ho ─ìinidla) b)
První derivace
potenciometrick├® k┼Öivky |
Autorsk├® pozn├ímky
Jaroslava Vávrová