Abstrakt
Tyrozin patÅà mezi neesenciÃĄlnà glukoplastickÃĐ i
ketoplastickÃĐ aminokyseliny. Tyrozin je prekurzorem pro biosyntÃĐzu hormonÅŊ
adrenalinu, thyroxinu a trijodthyroninu, zÃĄroveÅ pro biosyntÃĐzu melaninÅŊ
(pigmentÅŊ kÅŊÅūe, vlasÅŊ, vousÅŊ, oÄÃ), neurotransmitteru dopaminu, biochromÅŊ.
Terminologie
Tyrozin, 2-amino-3-(4-hydroxyfenyl)propionÃĄt
Synonyma
Tyrosin, 2-amino-3-(4-hydroxyfenyl)propionÃĄt
KlasifikaÄnà kÃģdy
Odkazy na jinÃĐ
relevantnà dokumenty, dalÅĄÃ informace
DÄdiÄnÃĐ
metabolickÃĐ poruchy aminokyselin
ChemickÃĄ a fyzikÃĄlnÃ
charakteristika, struktura a povaha analytu
Tyrozin (Tyr), NH2CH(CH2C6H4OH)COOH,
C9H11O3N
m.h. 181,2
KyselÃĄ disociaÄnà konstanta pK (25 oC)
2,20; 10,07(OH); 9,11
IzoelektrickÃ― bod pI 5,66
Tyrozin je neesenciÃĄlnà aminokyselina, tzv.
âpodmÃnÄnÄ postradatelnÃĄâ pouze pÅi dostatku esenciÃĄlnà aminokyseliny â
fenylalaninu. Podle chemickÃĐho charakteru jejÃho postrannÃho ÅetÄzce ji ÅadÃme
mezi polÃĄrnà aminokyseliny. PolÃĄrnà charakter dodÃĄvÃĄ tyrozinu fenolovÃĄ skupina,
dÃky svÃĐ schopnosti tvoÅit vodÃkovÃĐ vazby je souÄÃĄstà aktivnÃch center Åady
bÃlkovin.
AromatickÃ― kruh tyrozinu funguje jako chromofor a
absorbuje ultrafialovÃĐ zÃĄÅenà v oblasti vlnovÃ―ch dÃĐlek l 260-300
nm.Tyrozin obsahuje asymetrickÃ― atom uhlÃku, existuje proto ve dvou
enantiomernÃch konfiguracÃch â D a L, v bÃlkovinÃĄch se vyskytujà pouze
L-formy.
NÃĄzev tyrozin je odvozen podle sÃ―ra, Åecky tyros.
Role v metabolismu
Tyrozin je spolu s fenylalaninem prekurzorem
pro biosyntÃĐzu hormonÅŊ adrenalinu (dÅeÅ nadledvin), thyroxinu a trijodthyroninu
(ÅĄtÃtnÃĄ ÅūlÃĄza), dÃĄle pro biosyntÃĐzu melaninÅŊ (pigmentÅŊ kÅŊÅūe, vlasÅŊ, vousÅŊ,
oÄÃ). Tyrozin je zÃĄroveÅ prekurzorem Åady dÅŊleÅūitÃ―ch lÃĄtek â neurotransmitteru
dopaminu, biochromÅŊ.
Zdroj (syntÃĐza,
pÅÃjem)
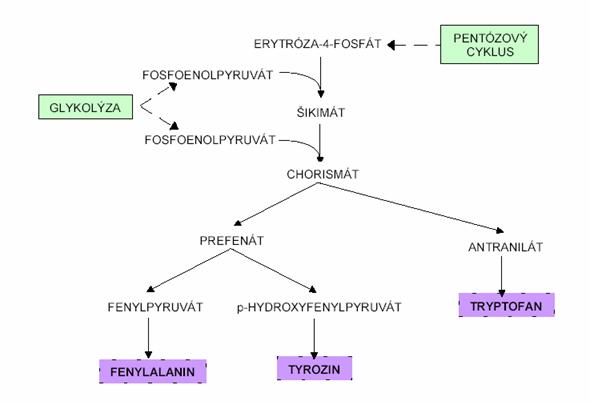
BiosyntÃĐza tyrozinu je spoleÄnÃĄ pro vÅĄechny
aromatickÃĐ aminokyseliny. BiosyntÃĐza aromatickÃ―ch aminokyselin zaÄÃnÃĄ
kondenzacà fosfoenolpyruvÃĄtu (meziprodukt glykolÃ―zy) a erytrÃģza-4-fosfÃĄtu
(meziprodukt regeneraÄnà fÃĄze pentÃģzovÃĐho cyklu). DÃĄle pÅes Åadu meziproduktÅŊ
vznikÃĄ ÅĄikimÃĄt, kterÃ― reaguje s dalÅĄÃm fosfoenolpyruvÃĄtem na chorismÃĄt.
Zde se cesta biosyntÃĐzy aromatickÃ―ch aminokyselin vÄtvÃ, biosyntÃĐze tyrozinu
probÃhÃĄ nÃĄsledovnÄ: z chorismÃĄtu vznikÃĄ prefenÃĄt, dÃĄle
p-hydroxyfenylpyruvÃĄt a z p-hydroxyfenylpyruvÃĄtu vznikÃĄ tyrozin. Tyrozin
mÅŊÅūe bÃ―t syntetizovÃĄn i hydroxylacà fenalaninu za katalÃ―zy
fenylalaninhydroxylÃĄzy.
PrÅŊmyslovÄ je tyrozin (stejnÄ jako vÄtÅĄina
aminokyselin) vyrÃĄbÄn biosyntÃĐzou uÅūitÃm mikroorganismÅŊ nebo chemickou syntÃĐzou
nebo kombinacà chemickÃĐ syntÃĐzy a rÅŊznÃ―ch biotechnologickÃ―ch postupÅŊ. Je
pouÅūÃvÃĄn jako souÄÃĄstà krmiv pro uÅūitkovÃĄ zvÃÅata, ochucovadlo potravin,
konzervaÄnà a antioxidaÄnà pÅÃpravky.
Distribuce v
organismu, obsah ve tkÃĄnÃch
Tyrozin je ubikvitnÃ
aminokyselina. ZvÃ―ÅĄenÃĐ hladiny jsou v krvi u novorozencÅŊ a nedonoÅĄencÅŊ.
NeonatÃĄlnà transitornà hypertyrozinÃĐmie je fyziologickÃĄ a zÅejmÄ
neÅĄkodnÃĄ.
DÄdiÄnÃĐ metabolickÃĐ
poruchy, kterÃĄ se Åadà mezi poruchy metabolismu tyrozinu jsou: hypertyrozinÃĐmie
typu I, hypertyrozinÃĐmie typu II,
hypertyrozinÃĐmie typu III.
Poruchy
odbourÃĄvÃĄnà tyrozinu.
ZpÅŊsob vyluÄovÃĄnà nebo
metabolismusOSN-E
Tyrozin patÅÃ mezi glukoplastickÃĐ i ketoplastickÃĐ
aminokyseliny. Hlavnà cesta odbourÃĄvÃĄnà tyrozinu je sloÅūitÃ― nÄkolikastupÅovÃ―
proces: tyrozin je transaminovÃĄn na 4-hydroxyfenylpyruvÃĄt, ze kterÃĐho pÅes
nÄkolik meziproduktÅŊ vznikÃĄ 4-fumarylacetoacetÃĄt. Ze 4-fumarylacetoacetÃĄtu je
odÅĄtÄpen fumarÃĄt, kterÃ― vstupuje do citrÃĄtovÃĐho cyklu a ze zbylÃĐho acetoacetÃĄtu
mohou bÃ―t syntetizovÃĄny mastnÃĐ kyseliny.
Literatura
Z.VodrÃĄÅūka: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie.
Academia, Praha 1987.
AutorskÃĐ poznÃĄmky
KarolÃna PeÅĄkovÃĄ
recenzoval Viktor KoÅūich