Abstrakt
Histidin patří mezi esenciální glukoplastické
aminokyseliny. Dva volné elektronové páry na atomech dusíku dodávají
postrannímu řetězci histidinu chelační schopnosti, takže tvoří snadno komplexy
s těžkými kovy. Dekarboxylací histidinu vzniká histamin – biogenní amin,
který má širokou škálu působení v organismu.
Terminologie
Histidin, 2-amino-1H-imidazol-4-propionát
Synonyma
2-amino-1H-imidazol-4-propionát
Klasifikační kódy
Odkazy na jiné relevantní dokumenty,
další informace
Dědičné metabolické
poruchy aminokyselin
Chemická a fyzikální
charakteristika, struktura a povaha analytu
Histidin (His), NH2CH(CH2Im)COOH,
C6H9O2N3
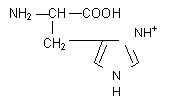
m.h. 155,2
Kyselá disociační konstanta pK (25 oC)
1,82; 6,0 (Im+); 9,17
Izoelektrický bod pI 7,59
Histidin je esenciální aminokyselina v době vývoje
v dětském věku, v dospělosti je postradatelná. Podle chemického
charakteru jejího postranního řetězce ji řadíme mezi bazické aminokyseliny a
mezi aminokyseliny s elektrickým nábojem na postranním řetězci, který se
podílí na elektrostatických interakcích. Postranní řetězec má pK blízké
fyziologickému pH, může proto spontánně přijímat protony i je poskytovat jiným
látkám, a tak fungovat jako součást nábojové štafety. Imidazolový kruh je
současně dobrým nukleofilem, a tak často tvoří katalytickou skupinu aktivních
center enzymů.
Histidin obsahuje asymetrický atom uhlíku, existuje
proto ve dvou enantiomerních konfiguracích – D a L, v bílkovinách se
vyskytují pouze L-formy.
Role v metabolismu
Dva volné elektronové páry na atomech dusíku dodávají
postrannímu řetězci histidinu chelační schopnosti, takže tvoří snadno komplexy
s těžkými kovy. Dekarboxylací histidinu vzniká histamin, histamin je
biogenní amin, který má širokou škálu působení v organismu. Účastní se
alergických reakcích, způsobuje kontrakci hladkého svalstva, stimuluje
vylučování katecholaminů a sekreci kyseliny chlorovodíkové buňkami žaludeční
sliznice.
Zdroj (syntéza, příjem)
Biosyntéza histidinu u savců není známa, u
mikroorganismů probíhá poměrně složitě. Biosyntéza začíná kondenzací ATP a
fosforibosyldifosfátu za vzniku N´-5-fosforibosyl-ATP. Z N´-5-fosforibosyl-ATP
se sledem reakcí vytvoří 5-aminoimidazol-4-karboxamidribonukleotid (meziprodukt
biosyntézy purinů) a imidazolglycerolfosfát. Z imidazolglycerolfosfátu
vzniká histidin.
Průmyslově je histidin (stejně jako většina
aminokyselin) vyráběn biosyntézou užitím mikroorganismů nebo chemickou syntézou
nebo kombinací chemické syntézy a různých biotechnologických postupů. Je
používán jako součástí krmiv pro užitková zvířata, ochucovadlo potravin, konzervační
a antioxidační přípravky.
Distribuce v organismu, obsah
ve tkáních
Histidin je
přítomen ve všech tkáních a tělních tekutinách, je to hlavní bazická
aminokyselina v moči. Zvýšené hodnoty jsou hlavně během gravidity.
K mírnému zvýšení hodnot v krvi dochází u histidinémie (OMIM *235800) - benigní dědičná metabolická poruchy z deficitu histidázy. Histidinurie provází všechny generalizované hyperaminoacidurie. Poruchy
metabolismu histidinu.
Způsob vylučování nebo
metabolismus
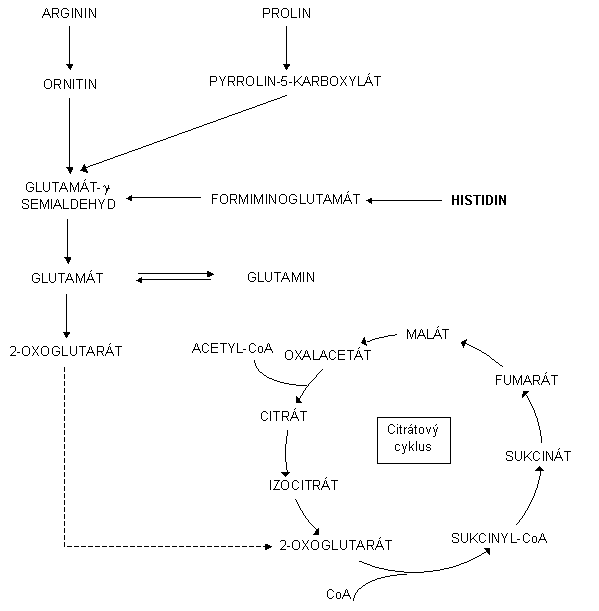
Histidin patří mezi glukoplastické aminokyseliny.
Histidin je přes několik meziproduktů (formiminoglutamát, glutamát-g-semialdehyd)
odbourán na glutamát. Glutamát je oxidační deaminací přeměně na 2-oxoglutarát.
2-oxoglutarát vstupuje do citrátového cyklu jako konečný produkt odbourávání
histidinu.
Literatura
Z.Vodrážka: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie. Academia,
Praha 1987.
Autorské poznámky
Karolína Pešková
recenzoval Josef Hyánek