Abstrakt
Arginin patří mezi esenciální glukoplastické
aminokyseliny. Biosyntéza argininu je součástí močovinového cyklu, arginin se
hydrolyticky štěpí na ornitin a ureu. Arginin tvoří protipól kyselých funkčních
skupin pro tvorbu solných můstků a pro vazbu aniontů a váže také kovalentně
karbonylové skupiny formou Schiffových bazí.
Terminologie
Arginin, 2-amino-5-guanidinovalerát
Synonyma
2-amino-5-guanidinovalerát
Odkazy na jiné relevantní
dokumenty, další informace
Arginin: parenterální
výživa
Argináza
Argininemie
Acidurie diabazická
Chemická a fyzikální
charakteristika, struktura a povaha analytu
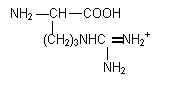
Arginin (Arg), NH2CH((CH2)
3Gua)COOH, C6H14O2N4
m.h. 174,2
Kyselá disociační konstanta pK (25 oC)
2,17; 9,04; 12,48(Gua+)
Izoelektrický bod pI 10,76
Arginin je esenciální aminokyselina v době vývoje
v dětském věku, v dospělosti je postradatelná. Podle chemického
charakteru jejího postranního řetězce ji řadíme mezi bazické aminokyseliny a
mezi aminokyseliny s elektrickým nábojem na postranním řetězci, který se
podílí na elektrostatických interakcích. Arginin má silně bazickou guanidilovou
skupinu, je to nejsilnější organická báze, srovnatelná s bazicitou NaOH.
Nese kladný náboj v celé oblasti stability většiny bílkovin.
Arginin obsahuje asymetrický atom uhlíku, existuje proto
ve dvou enantiomerních konfiguracích – D a L, v bílkovinách se vyskytují
pouze L-formy.
Role v metabolismu
Biosyntéza argininu je součástí močovinového cyklu,
arginin se hydrolyticky štěpí na ornitin a ureu. Arginin tvoří protipól
kyselých funkčních skupin pro tvorbu solných můstků a pro vazbu aniontů. Váže
také kovalentně karbonylové skupiny formou Schiffových bazí.
Arginin je intermediárním
metabolitem ureosyntetického cyklu, nepřímo souvisí s citrátovým cyklem a
s oxidačními ději při získávání energie. Arginin je esenciální pro
optimální buněčný růst in vitro, je prekurzorem biosyntézy polyaminů, které
jsou nezbytné pro proliferaci lymfocytů.
Fyziologicky v plazmě
jen ve stopách. Zvýšený při těžké dědičné poruše metabolismu - argininemii
z deficitu arginázy, dále u lysinové
intolerance a diabazické acidurii. Spolu
s cystinem, lysinem a ornitinem typická triáda pro klasickou cystinurii.
Zdroj (syntéza, příjem)
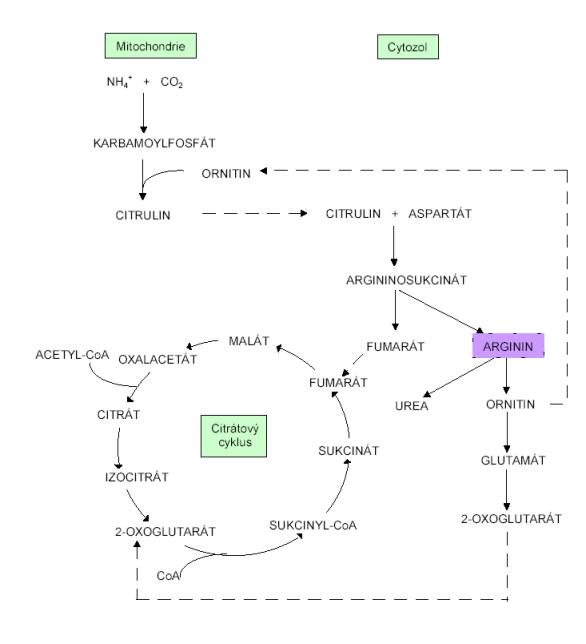
Biosyntéza argininu je součástí močovinového cyklu,
prekurzorem je ornitin. Karbamoylfosfát spolu s ornitinem tvoří citrulin,
citrulin reaguje s aspartátem (katalýza argininosukcinátsyntetázy) za vzniku
argininosukcinátu. Argininosukcinát se štěpí na arginin a fumarát. Fumarát
vstupuje do citrátového cyklu, umožňuje spojení močovinového a citrátového
cyklu.
Průmyslově je arginin (stejně jako většina aminokyselin)
vyráběn biosyntézou užitím mikroorganismů nebo chemickou syntézou nebo
kombinací chemické syntézy a různých biotechnologických postupů. Je používán
jako součástí krmiv pro užitková zvířata, ochucovadlo potravin, konzervační a antioxidační
přípravky.
Způsob vylučování nebo
metabolismus
Arginin patří mezi glukoplastické aminokyseliny. Arginin
je arginázou štěpen na ornitin a izoureu, izourea se spontánně přesmykne na
ureu a ornitin je přes glutamát-5-semialdehyd odbourán na glutamát. Glutamát je
oxidační deaminací přeměně na 2-oxoglutarát. 2-oxoglutarát vstupuje do
citrátového cyklu jako konečný produkt odbourávání argininu.
Literatura
Z.Vodrážka: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie. Academia,
Praha 1987.
Autorské poznámky
Karolína
Pešková
recenzoval
Josef Hynek