Abstrakt
Glutamin patří mezi neesenciální glukoplastické
aminokyseliny. Glutamin tvoří spolu s asparaginem latentní zásobu amoniaku
v organismech a hraje důležitou roli při využívání amoniaku v biosyntetických
dějích. Amidový dusík glutaminu se uplatňuje při různých reakcích – syntéza
aminokyselin transaminací, syntéza purinových nukleotidů, syntéza dalších
dusíkatých látek (histidin, glukosamin).
Glutamin, 2-amino-4-karbamidobutyrát
Synonyma
2-amino-4-karbamidobutyrát
Odkazy na jiné relevantní
dokumenty, další informace
Dědičné metabolické
poruchy aminokyselin
Glutamin: parenterální
výživa
Chemická a fyzikální
charakteristika, struktura a povaha analytu
Glutamin (Gln), NH2CH(CH2CH2CONH2)COOH,
C5H10O3N2
m.h. 146,1
Kyselá disociační konstanta pK (25 oC) 2,17; 9,13
Izoelektrický bod pI 5,65
Glutamin je neesenciální aminokyselina. Podle chemického
charakteru jejího postranního řetězce ji řadíme mezi polární aminokyseliny.
Polární funkční skupina glutaminu vytváří snadno polární interakce, zejména
vodíkové vazby, a to nejen mezi sebou navzájem, ale i s molekulami vody a
jinými nízkomolekulárními látkami. Glutamin zvyšuje rozpustnost bílkovin ve
vodě a prostorovým rozložením dipólů umožňuje specifickou vazbu větších
polárních molekul.
Glutamin obsahuje asymetrický atom uhlíku, existuje
proto ve dvou enantiomerních konfiguracích – D a L, v bílkovinách se
vyskytují pouze L-formy.
Role v metabolismu
Glutamin
je nejrozšířenější aminokyselina v krvi i ve volném poolu AK
v buňkách. Kosterní sval je hlavní tkání jeho syntézy, skladování a
uvolňování. Glutamin je zdrojem energie pro rychle rostoucí buňky, včetně
enterocytů, retikulocytů a lymfocytů.
Glutamin tvoří spolu s asparaginem latentní zásobu
amoniaku v organismech (ve volné formě) a hraje důležitou roli při
využívání amoniaku v biosyntetických dějích. Amidový dusík glutaminu se
uplatňuje při různých reakcích – syntéza aminokyselin transaminací, syntéza
purinových nukleotidů, syntéza dalších dusíkatých látek (histidin, glukosamin).
Detoxikace amoniaku probíhá následovně: amoniak je
detoxikován vazbou na glutamát, vzniká glutamin a ten je přenášen krví do
jater. V játrech odevzdá většinu amoniaku do močovinového cyklu a menší
část do ledvin, kde glutaminázou uvolněný amoniak neutralizuje kyseliny
vznikající v metabolismu a vylučuje se s nimi močí.
Glutamin a asparagin jsou stavební jednotky bílkovin,
ale také transportéry (lehce přechází přes buněčnou membránu). Glutamin může ve
vysoké koncentraci působit jako inhibitor vylučování fyziologických
nerotransmiterrů.
Metabolismus
glutaminu v katabolických stavech: cirkulující glutamin je snížen i přes
zvýšené uvolňování periferií. Je popisováno i snížení intracelulární
koncentrace glutaminu, které může nepříznivě ovlivnit metabolismus bílkovin ve
stresu. Je zrychlen příjem glutaminu některými tkáněmi, především střevem a
vychytávání glutaminu ledvinami se také zvyšuje. U sepse je deplece glutaminu
ještě těžší a delší než po traumatu. Při renálním selhání v sepsi se
naopak ledviny stávají orgánem uvolňujícím glutamin. Příjem střevem
v sepsi klesá a naopak stoupá příjem játry, která se stávají primárním
orgánem utilizace glutaminu při endotoxemii.
Zdroj (syntéza, příjem)
Glutamin se tvoří amidací glutamátu za katalýzy
glutaminsyntetázy.
Průmyslově je glutamin (stejně jako většina
aminokyselin) vyráběn biosyntézou užitím mikroorganismů nebo chemickou syntézou
nebo kombinací chemické syntézy a různých biotechnologických postupů. Je
používán jako součástí krmiv pro užitková zvířata, ochucovadlo potravin,
konzervační a antioxidační přípravky.
Distribuce v organismu, obsah
ve tkáních
Glutamin je přítomen ve všech tělesných tekutinách; je
to nejvýraznější aminokyselina v likvoru. V moči nacházíme zvýšené hodnoty u dědičné
hyperamonémie, při sekundárních a generalizovaných hyperaminoaciduriích (OMIM 234500), jako např. syndrom Lowe (OMIM 309000), choroba Hartnupova (OMIM *234500), aj.
Způsob vylučování nebo
metabolismus
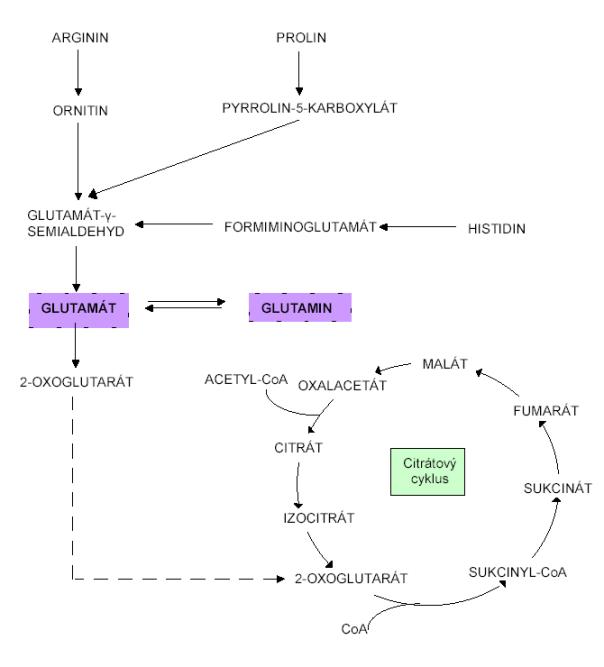
Glutamin patří mezi glukoplastické aminokyseliny,
v ledvinách je deamidován na glutamát za katalýzy glutaminázy. Glutamát je
oxidační deaminací přeměně na 2-oxoglutarát. 2-oxoglutarát vstupuje do
citrátového cyklu jako konečný produkt odbourávání glutaminu.
Literatura
Z.Vodrážka: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie. Academia,
Praha 1987.
Autorské poznámky
Karolína Pešková
recenzoval Josef Hyánek