Abstrakt
Serin patří mezi neesenciální glukoplastické
aminokyseliny, uplatňuje se v řadě biochemických reakcích. Serin tvoří
jako součást fosfoacylglycerolů stavební součást biologických membrán, účastní
se aktivace fosforylázy a je součástí chymotrypsinu.
Terminologie
Serin, 2-amino-3-hydroxypropionát
Synonyma
2-amino-3-hydroxypropionát
Klasifikační kódy
Odkazy na jiné
relevantní dokumenty, další informace
Chemická a fyzikální
charakteristika, struktura a povaha analytu
Serin (Ser), NH2CH(CH2OH)COOH,
C3H7O3N
m.h. 105,1
Kyselá disociační konstanta pK (25 oC)
2,21; 9,15
Izoelektrický bod pI 5,68
Serin je neesenciální aminokyselina. Podle
chemického charakteru jejího postranního řetězce (-OH) ji řadíme mezi polární
aminokyseliny. Polární funkční skupina serinu vytváří snadno polární interakce,
zejména vodíkové vazby, a to nejen mezi sebou navzájem, ale i s molekulami
vody a jinými nízkomolekulárními látkami. Serin zvyšuje rozpustnost bílkovin ve
vodě a prostorovým rozložením dipólů umožňuje specifickou vazbu větších
polárních molekul.
Serin obsahuje asymetrický atom uhlíku, existuje
proto ve dvou enantiomerních konfiguracích – D a L, v bílkovinách se vyskytují
pouze L-formy.
Role v metabolismu
Serin se uplatňuje v řadě biochemických
reakcích, díky schopnosti tvořit vodíkové interakce a reagovat za vhodných
podmínek jako nukleofil. Serin je složkou řady glykosidových vazeb
glykoproteinů, esterových vazeb fosfoproteinů a fosfoacylglycerolů.
Fosfoacylglyceroly jsou stavebním základem biologických membrán.
Spolu s treoninem má serin velký význam při
aktivaci či inaktivaci enzymů, které jsou regulovány hormony pomocí druhotného
přenašeče cyklického 3´,5´-adenozinmonofosfátu. Serin a treonin zde fungují
jako příjemci fosforylové skupiny.
Zdroj (syntéza, příjem)
Serin se tvoří v organismu převážně z
3-fosfoglycerátu (meziproduktu glykolýzy). Dehydrogenací 3-fosfoglycerátu
vzniká 3-fosfohydroxypyruvát, který je transaminován na 3-fosfoserin, který je
hydrolyzován na serin. Serin je prekurzorem biosyntézy glycinu a cysteinu.
Průmyslově je serin (stejně jako většina
aminokyselin) vyráběn biosyntézou užitím mikroorganismů nebo chemickou syntézou
nebo kombinací chemické syntézy a různých biotechnologických postupů. Je
používán jako součástí krmiv pro užitková zvířata, ochucovadlo potravin,
konzervační a antioxidační přípravky.
Distribuce v
organismu, obsah ve tkáních
Snížené hladiny
serinu v krvi a likvoru se nalézají při dědičné metabolické poruše biosyntézy
serinu - deficitu 3-fosfoglycerátdehydrogenázy.
Poruchy
metabolismu glycinu a serinu.
Způsob vylučování nebo
metabolismusOSN-E
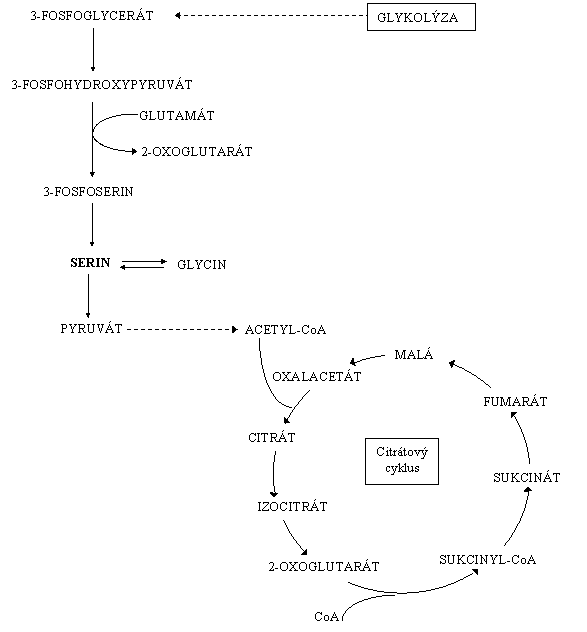
Serin patří mezi
glukoplastické aminokyseliny. Odbourávání serinu probíhá jednoduchou přímou
cestou na pyruvát. Pyruvát je oxidační dekarboxylací přeměněn na acetylkoenzym
A (acetylCoA). AcetylCoA vstupuje do citrátového cyklu jako konečný produkt
odbourávání serinu.
Literatura
Z.Vodrážka: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie.
Academia, Praha 1987.
Autorské poznámky
Karolína Pešková
recenzoval Viktor Kožich