Abstrakt
Tryptofan patří mezi esenciální glukoplastické i
ketoplastické aminokyseliny. Tryptofan je výchozí látkou při biosyntéze řady
důležitých látek, např. serotoninu, nikotinamidu. Většina tryptofanu se
spotřebuje pro syntézu bílkovin, část je metabolizována na biogenní látky
indolového nebo pyridinového skeletu.
Terminologie
Tryptofan
Synonyma
Klasifikační kódy
Odkazy na jiné
relevantní dokumenty, další informace
Dědičné
metabolické poruchy aminokyselin
Chemická a fyzikální
charakteristika, struktura a povaha analytu
Tryptofan (Trp), NH2CH(CH2C8H5NH)COOH,
C11H12O2N2
m.h. 204,2
Kyselá disociační konstanta pK (25 oC)
2,38; 9,39
Izoelektrický bod pI 5,89
Tryptofan je esenciální aminokyselina, tzn. nelze
ji v organizmu syntetizovat, musí se získat potravou nebo štěpením
tkáňových bílkovin. Jen stopy tryptofanu se tvoří ve střevě účinkem bakterií.
Podle chemického charakteru jejího postranního řetězce ji řadíme mezi nepolární
aminokyseliny. Postranní řetězec se uplatňuje v hydrofobních interakcích
bílkovin. Aromatický kruh tryptofanu funguje jako chromofor a absorbuje
ultrafialové záření v oblasti vlnových délek l=260-300 nm.
Tryptofan obsahuje asymetrický atom uhlíku,
existuje proto ve dvou enantiomerních konfiguracích – D a L, v bílkovinách
se vyskytují pouze L-formy.
Role v metabolismu
Tryptofan je výchozí látkou při biosyntéze řady
důležitých látek, např. serotoninu, nikotinamidu. Většina tryptofanu se
spotřebuje pro syntézu bílkovin, část je metabolizována na biogenní látky
indolového nebo pyridinového skeletu.
Zdroj (syntéza,
příjem)
Tryptofan patří mezi esenciální aminokyseliny,
nelze ji tedy v organizmu syntetizovat. Její biosyntéza probíhá vesměs jen
u rostlin a mikroorganismů a je společná pro všechny aromatické aminokyseliny.
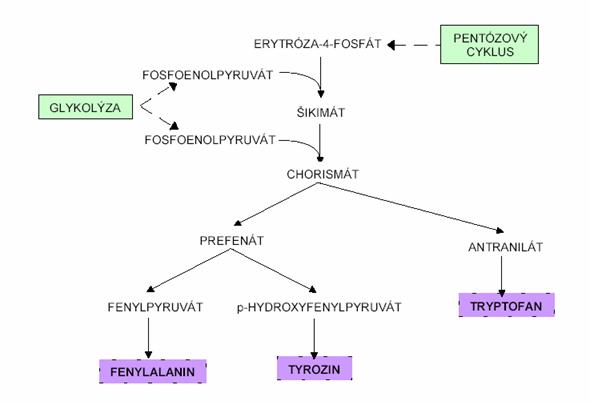
Biosyntéza aromatických aminokyselin začíná kondenzací fosfoenolpyruvátu
(meziprodukt glykolýzy) a erytróza-4-fosfátu (meziprodukt regenerační fáze
pentózového cyklu). Dále přes řadu meziproduktů vzniká šikimát, který reaguje
s dalším fosfoenolpyruvátem na chorismát. Zde se cesta biosyntézy
aromatických aminokyselin větví, biosyntéze tryptofanu probíhá následovně:
z chorismátu vzniká antranilát, jeho reakcí s fosforibosyldifosfátem
vzniká tryptofan.
Průmyslově je tryptofan (stejně jako většina
aminokyselin) vyráběn biosyntézou užitím mikroorganismů nebo chemickou syntézou
nebo kombinací chemické syntézy a různých biotechnologických postupů. Je
používán jako součástí krmiv pro užitková zvířata, ochucovadlo potravin,
konzervační a antioxidační přípravky. Tryptofan má antidepresivní účinky, je
součástí některých léků užívaných při léčbě alkoholismu a nespavosti.
Distribuce v
organismu, obsah ve tkáních
Tryptofan je v plasmě je vázán na albumin. Mezi dědičné poruchy metabolismu tryptofanu
patří: hydroxykynureninurie; malabsorpce tryptofanu; Hartnupova choroba.
Poruchy metabolismu tryptofanu.
Způsob vylučování nebo
metabolismusOSN-E
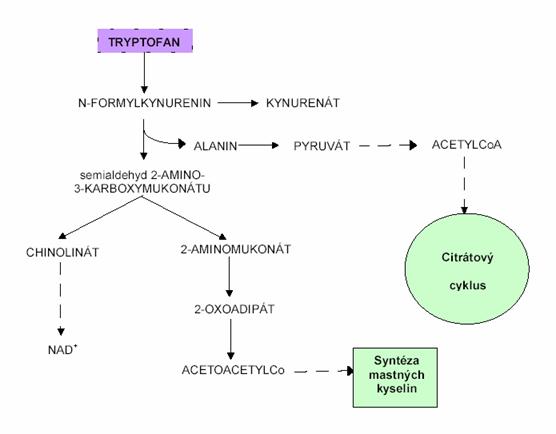
Tryptofan patří mezi glukoplastické i
ketoplastické aminokyseliny. Hlavní cesta odbourávání tryptofanu začíná
oxidačním štěpením pyrrolového kruhu za vzniku N-formylkynureninu, který je buď
transaminován na kynurenát nebo odbourán na alanin a semialdehyd
2-amino-3-karboxymukonátu. Od tohoto meziproduktu pokračují 2 různé cesty:
jedna vede po spontánní cyklizaci k NAD+, druhou je kompletní
oxidační odbourání tryptofanu na CO2 a H2O, přes
acetylkoenzym A a citrátový cyklus.
Literatura
Z.Vodrážka: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie.
Academia, Praha 1987.
Autorské poznámky
Karolína Pešková
recenzoval Viktor Kožich