Abstrakt
Z√°kladn√≠ princip plynov√© chromatografie spońć√≠v√° v tom,
Ňĺe mobiln√≠ f√°ze je plynn√° a separovan√© sloŇĺky jsou rovnńõŇĺ ve stavu plynn√©m.
Stacion√°rn√≠ f√°ze (pevn√° l√°tka nebo kapalina) pŇĮsob√≠ selektivnńõ, na z√°kladńõ vz√°jemn√Ĺch
interakc√≠ stacion√°rn√≠ f√°ze-vzorek doch√°z√≠ k rozdńõlen√≠ a detekci analyzovan√Ĺch
komponent.
Související informace
chromatografie, plynová chromatografie, stacionární fázeKEY-E, mobilní
f√°ze, pneumatick√© obvody, d√°vkovac√≠ zaŇô√≠zen√≠, n√°plŇąov√© kolonyKEY-E, kapil√°rn√≠
kolony, detektor
Text
Text je ńćlenńõn dle osnovy:
A.
Pneumatické
obvody
A.- 1. Zdroje nosného plynu a
pomocn√Ĺch plynŇĮ
A.- 2. ńĆiŇ°tńõn√≠ plynŇĮ
A.- 3. Regulace a mńõŇôen√≠ tlaku
a prŇĮtoku nosn√©ho plynu
B.
Dávkovací
zaŇô√≠zen√≠
C.
Kolony
C.- 1.¬† N√°plŇąov√© kolony
C.- 2.  Kapilární kolony
D.
Detekńćn√≠
systém
D.- 1. Tepelnńõ vodivostn√≠
detektor (TCD)
D.- 2. Plamenov√Ĺ ionizańćn√≠
detektor (FID)
D.- 3. Termoionizańćn√≠
selektivní  detektor (TSD,AFID, NPD)
D.- 4. Fotoionizańćn√≠ detektor
(PID)
D.- 5. Heliov√Ĺ detektor (HeD)
D.- 6. Detektor elektronového
z√°chytu (ECD)
D.- 7. Hmotnostní detekce
(GC-MS)
E. Termostaty
F. Zpracování signálu detektoru a ostatních informací
G. PŇô√≠prava vzorkŇĮ
Plynov√° chromatografie - √ļvod
Maj√≠-li b√Ĺt hodnoty namńõŇôen√© metodou plynov√©
chromatografie objektivnńõ reprodukovateln√© a spr√°vn√©, mus√≠ platit definovan√©
tlakov√©, tokov√© a teplotn√≠ parametry cel√©ho pŇô√≠stroje. PŇô√≠stroj pro plynovou
chromatografii je z tohoto hlediska syst√©mem nńõkolika obvodŇĮ:
-
Pneumatické
obvody (zdroje nosn√©ho plynu a pomocn√Ĺch plynŇĮ, zaŇô√≠zen√≠ pro ńćiŇ°tńõn√≠, regulaci,
mńõŇôen√≠ tlaku a prŇĮtoku plynŇĮ)
-
Dávkovací
zaŇô√≠zen√≠
-
Kolony
-
Detekńćn√≠
systém
-
Termostaty
-
Zpracování
signálu detektoru a ostatních informací
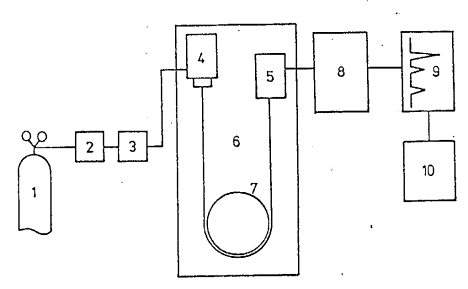
1)
zdroj
nosného plynu
2)
ńćiŇ°tńõn√≠
plynu
3)
regulace
4)
dávkovací
zaŇô√≠zen√≠
5)
detektor
6)
termostat
7)
separańćn√≠
kolona
8)
zesilovańć
sign√°lu
9)
v√Ĺstup
dat
A. Pneumatické obvody
A.- 1. Zdroje nosn√©ho plynu a pomocn√Ĺch plynŇĮ.
Jako nosn√Ĺ plyn mŇĮŇĺe b√Ĺt pouŇĺit kaŇĺd√Ĺ plyn o vhodn√Ĺch
vlastnostech, mus√≠ b√Ĺt dostateńćnńõ ńćist√Ĺ, vhodn√Ĺ pro pouŇĺit√Ĺ detektor, inertn√≠ vŇĮńći
stacion√°rn√≠ f√°zi, analyzovan√Ĺm l√°tk√°m a materi√°lu tńõch ńć√°st√≠ chromatografu, se
kter√Ĺmi pŇôijde do styku. Pomocn√© plyny umoŇĺŇąuj√≠ funkci detektorŇĮ, d√°vkov√°n√≠,
chlazen√≠. BńõŇĺnńõ pouŇĺ√≠van√Ĺmi nosn√Ĺmi plyny jsou dus√≠k, argon, helium, vod√≠k,
mezi pomocn√© plyny patŇô√≠ obvykle vzduch, kysl√≠k, vod√≠k, oxid uhlińćit√Ĺ, oxid
dusn√Ĺ. Zdrojem nosn√©ho i pomocn√©ho plynu jsou vńõtŇ°inou ocelov√© tlakov√© lahve
naplnńõn√© pŇô√≠sluŇ°n√Ĺm plynem. Jin√Ĺm zdrojem plynŇĮ jsou i komerńćnńõ dod√°van√©
speci√°ln√≠ elektrolyz√©ry pro vod√≠k, kysl√≠k oxid uhlińćit√Ĺ aj., popŇô√≠padńõ
kompresory na vzduch.
A.- 2. ńĆiŇ°tńõn√≠ plynŇĮ.
PŇôi stopov√© anal√Ĺze, pŇôi pouŇĺit√≠ stacion√°rn√≠ch f√°z√≠
citliv√Ĺch na kysl√≠k, vodu aj. a pŇôi pr√°ci s kolonou za vyŇ°Ň°√≠ch teplot se mus√≠
nosn√Ĺ plyn ńćistit. Zbavuje se vodn√≠ p√°ry, kysl√≠ku, niŇĺŇ°√≠ch uhlovod√≠kŇĮ apod., a
to fyzik√°ln√≠m i chemick√Ĺm zpŇĮsobem nebo kombinac√≠ obou. K suŇ°en√≠ plynŇĮ se
pouŇĺ√≠vaj√≠ pŇôedevŇ°√≠m molekulov√° s√≠ta, silikagel nebo aktivn√≠ uhl√≠. Kysl√≠k a
dalŇ°√≠ neńćistoty lze z nosn√©ho plynu odstranit reakc√≠ se speci√°ln√≠mi
katalyz√°tory. Komerńćnńõ jsou dod√°v√°ny trubice se vhodnou n√°pln√≠, kter√© se um√≠st√≠
v cestńõ mezi zdroj plynu a jeho vstup do separańćn√≠ho syst√©mu plynov√©ho
chromatografu.
A.- 3. Regulace a mńõŇôen√≠ tlaku a prŇĮtoku nosn√©ho
plynu
Komerńćnńõ dod√°van√© chromatografy b√Ĺvaj√≠ vybaveny regul√°tory
tlaku a prŇĮtoku pro vŇ°echny pouŇĺ√≠van√© plyny, v dokonalejŇ°√≠m zapojen√≠ pak
kombinac√≠ regul√°toru prŇĮtoku se zpńõtn√Ĺm regul√°torem tlaku. PouŇĺ√≠vaj√≠ se napŇô.
regul√°tory membr√°nov√© nebo regul√°tory s vlnovcem. Tlaky v plynech se mńõŇô√≠
celokovov√Ĺmi manometry s odpov√≠daj√≠c√≠m rozsahem a pŇôesnost√≠. Pro regulaci
tlakŇĮ, resp. prŇĮtokŇĮ, se sn√≠maj√≠ tlaky tenzometrick√Ĺmi ńćidly napojen√Ĺmi na
mikroprocesor.
B. D√°vkovac√≠ zaŇô√≠zen√≠
D√°vkovac√≠ zaŇô√≠zen√≠ se obvykle nach√°z√≠ ve vymńõniteln√©m v√≠ku
termostatu co nejbl√≠Ňĺe vstupu do kolony. Vzorek se vn√°Ň°√≠ buńŹ do proudu nosn√©ho
plynu nebo pŇô√≠mo do kolony. Volba d√°vkovac√≠ho procesu je urńćena jak typem
pouŇĺit√© kolony, tak vlastnostmi analyzovan√Ĺch l√°tek. Aby byla maxim√°lnńõ vyuŇĺita
separańćn√≠ √ļńćinost kolony, je tŇôeba d√°vkovat mal√° mnoŇĺstv√≠ vzorku, kter√°
pŇôich√°z√≠ na kolonu v plynn√©m stavu v ostr√© z√≥nńõ. Teplota n√°stŇôikov√©ho bloku se
vol√≠ zpravidla asi o 50¬įC vyŇ°Ň°√≠ neŇĺ je bod varu nejv√ĹŇ°e vrouc√≠ sloŇĺky
analyzovan√© smńõsi.
D√°vkovac√≠ proces se skl√°d√° z nńõkolika krokŇĮ:
-
odmńõŇôen√≠
vzorku (mikrostŇô√≠kańćka, kalibrovan√° kapil√°ra, obtokov√© d√°vkovańće, kapil√°ry),
-
zavedení
do n√°stŇôikov√© ńć√°sti chromatografu nebo aŇĺ do kolony,
-
rychlého
odpaŇôen√≠ vzorku nebo jeho rozpt√Ĺlen√≠ do aerosolov√©ho stavu,
-
transportu
odpaŇôen√©ho vzorku z n√°stŇôikov√© ńć√°sti nosn√Ĺm plynem do kolony.
D√°vkovac√≠ zaŇô√≠zen√≠ by mńõlo splŇąovat kriteria:
-
rychl√Ĺ
pŇôevod kapaln√Ĺch a tuh√Ĺch vzorkŇĮ do plynn√©ho stavu,
-
bńõhem
pŇôevodu do plynn√©ho stavu by nemńõlo doch√°zet ke zmńõn√°m ve sloŇĺen√≠ vzorku,
-
dávkování
by nemńõlo zpŇĮsobovat tlakov√© r√°zy a poruŇ°ovat rovnov√°Ňĺn√© pomńõry v kolonńõ,
-
klasick√Ĺ
zpŇĮsob d√°vkov√°n√≠ do kapil√°rn√≠ch kolon pŇôedpokl√°d√°, Ňĺe mnoŇĺstv√≠ a objem vzorku
nepŇôes√°hne kapacitu kolony.
D√°vkov√°n√≠ plynŇĮ:
-
plynov√Ĺmi
byretami,
-
plynotńõsn√Ĺmi
injekńćn√≠mi stŇô√≠kańćkami,
-
obtokov√Ĺmi
dávkovacími kohouty.
D√°vkov√°n√≠ kapalin a tuh√Ĺch l√°tek: - mikrostŇô√≠kańćky
Vzorky s vysokou koncentrací analyzované látky, viskózní
kapaliny a tuh√© vzorky se d√°vkuj√≠ v roztoc√≠ch tńõkav√Ĺch rozpouŇ°tńõdel.
Automatick√° d√°vkovac√≠ zaŇô√≠zen√≠:
PŇôi d√°vkov√°n√≠ plynŇĮ se pouŇĺ√≠v√° Ňôada obtokov√Ĺch syst√©mŇĮ,
kter√© mohou d√°vkovat zvolen√° mnoŇĺstv√≠ v urńćit√©m ńćasov√©m intervalu. V syst√©mu
zaŇôazen√© v√≠cecestn√© kohouty jsou ovl√°d√°ny pneumaticky. Kapaln√© l√°tky a roztoky
jsou d√°vkov√°ny jako takov√© nebo ve formńõ par odeb√≠ran√Ĺch nad kapalinou
automatick√Ĺmi d√°vkovańći, kter√© pracuj√≠ na injekńćn√≠m principu. D√°vkovac√≠
zaŇô√≠zen√≠ umoŇĺŇąuje pouŇĺ√≠t d√°vkov√°n√≠ s dńõlińćem toku nebo bez nńõj, injektor s
programovanou teplotou, d√°vkovat vzorek do kolony (on-column), d√°vkovat z
pŇôedkolony nebo d√°vkovat z pyrolyz√©ru. Volba zaŇô√≠zen√≠ a zpŇĮsobu d√°vkov√°n√≠
z√°vis√≠ na typu vzorku, koncentraci stanovovan√Ĺch l√°tek, jejich tńõkavosti, bodu
varu a tepelné i chemické stálosti.
C. Kolony
Kolona je povaŇĺov√°na za srdce chromatografu a na jej√≠m
v√Ĺbńõru z√°vis√≠ √ļspńõch anal√Ĺzy. PouŇĺ√≠vaj√≠ se dva z√°kladn√≠ typy kolon - n√°plŇąov√© a
kapil√°rn√≠. Do roku 1957 se pouŇĺ√≠valy pouze n√°plŇąov√© kolony s rŇĮzn√Ĺmi typy
sorbentŇĮ, po roce 1957 se zańćaly uplatŇąovat kolony kapil√°rn√≠, jejichŇĺ pouŇĺit√≠
pŇôi souńćasn√© instrumentaci pŇôevl√°d√°.
C.- 1. 
N√°plŇąov√© kolony:
N√°plŇąov√© kolony jsou sklenńõn√© nebo kovov√© trubice o
vnitŇôn√≠m prŇĮmńõru 2 - 5 mm (nejńćastńõji 2 mm) naplnńõn√© buńŹ adsorbentem (GSC) nebo
nosińćem smońćen√Ĺm zvolenou stacion√°rn√≠ f√°z√≠ (GLC). D√©lky kolon o vnitŇôn√≠m
prŇĮmńõru 2 mm se pohybuj√≠ v rozmez√≠ 0,9 - 3,5 m, preferuj√≠ se kolony sklenńõn√© se
silylovan√Ĺm vnitŇôn√≠m povrchem. Vzhledem k omezen√©mu prostoru termostatu, v nńõmŇĺ
je kolona um√≠stńõna, tvaruj√≠ se n√°plŇąov√© kolony obvykle do spir√°ly.
Adsorbenty pro GSC:
Adsorbenty se dńõl√≠ na z√°kladńõ mezimolekul√°rn√≠ch
interakc√≠ na nespecifick√© a specifick√©. Nespecifick√Ĺm adsorbentem mŇĮŇĺe b√Ĺt
napŇô. aktivn√≠ uhl√≠, specifick√Ĺmi jsou silikagel, alumina, molekulov√° s√≠ta aj.
Nosińće pro GSC:
NejrozŇ°√≠ŇôenńõjŇ°√≠mi nosińći v plynov√© chromatografii jsou rŇĮznńõ
upraven√© kŇôemeliny. Nev√Ĺhodou tńõchto nosińćŇĮ je pŇô√≠tomnost aktivn√≠ch center
(silanolov√© a siloxanov√© skupiny), kter√° zpŇĮsobuj√≠ neŇĺ√°douc√≠ chvostov√°n√≠
pol√°rnńõjŇ°√≠ch sloŇĺek vzorku pŇôi separaci. Potlańćen√≠ vlivu silanolov√Ĺch skupin se
prov√°d√≠ silylac√≠, kter√© pŇôedch√°z√≠ kysel√© pran√≠ nosińće.
C.- 2. 
Kapilární kolony
PŇôev√°Ňĺn√° vńõtŇ°ina aplikac√≠ se prov√°d√≠ na kŇôemenn√Ĺch
kapil√°rn√≠ch kolon√°ch. Jako stacion√°rn√≠ f√°ze se pouŇĺ√≠vaj√≠ univerz√°lnńõ ńćasto
nepolární silikonové fáze (SE-30, OV-1, SE-52 apod.) nebo imobilizované fáze
Carbowaxu.
Kolony s tenkou vrstvou stacionární fáze Kolony, kde
stacion√°rn√≠ f√°ze je fixov√°na na vnitŇôn√≠ stńõnńõ jako tenk√° vrstvińćka adsorbentu
nebo smońćen√©ho inertn√≠ho nosińće, zn√°m√© jsou pod oznańćen√≠m:
-
PLOT
(Porous Layer Open Tubular),
-
SCOT
(Support Coated Open Tubular).
Kapil√°rn√≠ kolony se siln√Ĺm filmem stacion√°rn√≠ f√°ze -
SCOT a PLOT kolony jsou nahrazovány kolonami s filmem stacionární fáze o
tlouŇ°Ň•ce jednotek aŇĺ des√≠tek mikrometrŇĮ. Zvl√°dnut√° technika imobilizace
stacion√°rn√≠ch f√°z√≠ pomoc√≠ prostorov√©ho zes√≠tńõn√≠ rŇĮzn√Ĺch stacion√°rn√≠ch f√°z√≠
zaruńćuje st√°lost tohoto typu kolon.
D. Detekńćn√≠ syst√©m
Chromatografick√Ĺ detektor by mńõl b√Ĺt citliv√Ĺ, stabiln√≠,
mńõl by zajiŇ°Ň•ovat maxim√°ln√≠ rychlost odezvy na zmńõnu ve sloŇĺen√≠ plynu
opouŇ°tńõj√≠c√≠ho chromatografickou kolonu. Mezi z√°kladn√≠ detektory se pońć√≠t√°
tepelnńõ vodivostn√≠, plamenov√Ĺ ionizańćn√≠, plamenov√Ĺ ionizańćn√≠ s alkalick√Ĺm
kovem, detektor elektronového záchytu.
D.- 1. Tepelnńõ vodivostn√≠ detektor (TCD):
Jedná se o universální nedestruktivní detektor, je
citliv√Ĺ k plynŇĮm s n√≠zkou molekulovou hmotnost√≠. Tepelnńõ vodivostn√≠ detektor se
skl√°d√° z platinov√© spir√°lky zasunut√© do komŇĮrky v kovov√©m bloku. Spir√°lkou
proch√°z√≠ konstantn√≠ proud, kter√Ĺ ji Ňĺhav√≠. PrŇĮtokem samotn√©ho nosn√©ho plynu je
teplota spir√°lky ust√°lena. JestliŇĺe se v nosn√©m plynu objev√≠ sloŇĺka vzorku
vystupuj√≠c√≠ z kolony, dojde ke zmńõnńõ odvodu tepla a t√≠m ke zmńõnńõ teploty
spir√°lky, coŇĺ vyvol√° √ļmńõrnou zmńõnu elektrick√©ho odporu. TCD jsou konstruov√°ny
obvykle se dvńõma spir√°lkami, pŇôes mńõrnou proch√°z√≠ nosn√Ĺ plyn s rozdńõlen√Ĺmi
sloŇĺkami vzorku, pŇôes druhou, referentn√≠ ńć√°st proch√°z√≠ pouze ńćist√Ĺ nosn√Ĺ plyn.
Pro tento typ detektoru vyhovuje nejl√©pe pouŇĺit√≠ nosn√Ĺch plynŇĮ s dobrou
tepelnou vodivost√≠, coŇĺ jsou pŇôedevŇ°√≠m vod√≠k a helium.
D.- 2. 
Plamenov√Ĺ ionizańćn√≠ detektor (FID):
Plamenov√Ĺ ionizańćn√≠ detektor se Ňôad√≠ do z√°kladn√≠ v√Ĺbavy
plynového chromatografu. Jedná se o destruktivní detektor. Princip detekce
spońć√≠v√° v mńõŇôen√≠ zmńõny ionizańćn√≠ho proudu vod√≠kov√©ho plam√≠nku v dŇĮsledku
pŇô√≠tomnosti eluovan√© sloŇĺky vzorku. Vznikl√© ionizovan√© ńć√°stice zaplŇąuj√≠ prostor
mezi elektrodami a sniŇĺuj√≠ jeho odpor, takŇĺe mŇĮŇĺe proch√°zet proud. FID d√°v√°
dostateńćnńõ velkou odezvu na t√©mńõŇô vŇ°echny organick√© l√°tky. BńõŇĺnńõ uŇĺ√≠van√© nosn√©
plyny d√°vaj√≠ n√≠zkou, t√©mńõŇô neregistrovatelnou odezvu. FID m√° nejvńõtŇ°√≠ line√°rn√≠
rozsah z bńõŇĺnńõ uŇĺ√≠van√Ĺch detektorŇĮ.
D.- 3. Termoionizańćn√≠ selektivn√≠ detektor (TSD,
AFID, NPD)
Tento typ detektoru je modifikací FID, jedná se o
selektivn√≠ termoionizańćn√≠ detektor s alkalick√Ĺm kovem (AFID). Modifikace spońć√≠v√°
v um√≠stńõn√≠ perlińćky nebo prstence se sol√≠ alkalick√©ho kovu v prostoru hoŇô√°ńćku
(pouŇĺ√≠vaj√≠ se hlavnńõ s√≠ran sodn√Ĺ, chlorid draseln√Ĺ, bromid cesn√Ĺ, chlorid
rubidn√Ĺ), detekce je zaloŇĺena na ionizaci alkalick√©ho kovu vlivem spalin
organick√© l√°tky. Detektor je zn√°m tak√© jako dus√≠k/fosfor (NPD), protoŇĺe doch√°z√≠
k selektivn√≠ ionizaci organick√Ĺmi slouńćeninami obsahuj√≠c√≠mi atomy dus√≠ku nebo
fosforu.
D.- 4. Fotoionizańćn√≠ detektor (PID)
Fotoionizańćn√≠ detektor je rovnńõŇĺ modifikac√≠ FID
detektoru. Energie pro ionizaci je z√≠sk√°v√°na prostŇôednictv√≠m UV lampy. Detektor
je jen zŇô√≠dka vyuŇĺ√≠v√°n, protoŇĺe m√° niŇĺŇ°√≠ mez detekce neŇĺ FID.
D.- 5. Heliov√Ĺ detektor (HeD):
ńĆinnost detektoru je zaloŇĺena na ionizaci sloŇĺky vzorku
do nńõj vstupuj√≠c√≠ z kolony atomy helia vybuzen√Ĺmi do metastabiln√≠ho stavu o
vysok√©m ionizańćn√≠m potenci√°lu. Detektor je vyuŇĺ√≠v√°n pŇôedevŇ°√≠m pŇôi anal√Ĺz√°ch
permanentn√≠ch plynŇĮ.
D.- 6. Detektor elektronového záchytu (ECD):
Jako nosn√Ĺ plyn se u tohoto typu detektoru pouŇĺ√≠v√° dus√≠k
nebo argon, oba plyny se snadno ionizuj√≠ mńõkk√Ĺm beta-z√°Ňôen√≠m (zdrojem b√Ĺv√°
tricium nebo 63Ni). V ionizovan√©m nosn√©m plynu jsou pŇô√≠tomny pouze elektrony
zachytiteln√© n√≠zk√Ĺm elektrodov√Ĺm potenci√°lem. Obsahuje-li nosn√Ĺ plyn sloŇĺku s
velkou elektronovou afinitou, dojde k pohlcen√≠ nńõkter√Ĺch energeticky chud√Ĺch
elektronŇĮ, pohyblivost tńõchto novńõ vznikl√Ĺch z√°pornńõ nabit√Ĺch ńć√°stic je mnohem
menŇ°√≠ ve srovn√°n√≠ s voln√Ĺmi elektrony a je tedy vyŇ°Ň°√≠ pravdńõpodobnost jejich
sr√°Ňĺky s kladnńõ nabit√Ĺmi ńć√°sticemi. Rekombinac√≠ dojde ke sn√≠Ňĺen√≠ celkov√©ho pońćtu
negativn√≠ch ńć√°stic a t√≠m i ke sn√≠Ňĺen√≠ hodnoty ionizańćn√≠ho proudu.
D.- 7. Hmotnostní detekce (GC-MS):
Spojení plynového chromatografu s hmotnostní detekcí je
urńćena samostatn√° kapitola.
E. Termostaty
Jednou z kritick√Ĺch velińćin v plynov√© chromatografii je
teplota a jej√≠ stabilita, na n√≠ z√°vis√≠ pŇôesnost a reprodukovatelnost mńõŇôen√Ĺch
√ļdajŇĮ. Je nutno udrŇĺovat zvolen√Ĺ konstantn√≠ teplotn√≠ reŇĺim n√°stŇôiku, kolony,
detektoru a regul√°toru tlaku a prŇĮtoku. Termostat by mńõl umoŇĺŇąovat udrŇĺovat
teplotu v rozmez√≠ 100 - 500 ¬įC. TeplovzduŇ°n√© termostaty jsou vybaveny nucenou
cirkulac√≠ vzduchu, coŇĺ umoŇĺŇąuje prov√°dńõt rychl√© zmńõny teploty. U vńõtŇ°iny
aplikac√≠ metod plynov√© chromatografie se uplatŇąuje postup s programovanou
zmńõnou teploty, reprodukovatelnost teplotn√≠ho gradientu se odr√°Ňĺ√≠ pŇôedevŇ°√≠m ve
stabilitńõ retenńćn√≠ch ńćasŇĮ p√≠kŇĮ jednotliv√Ĺch sloŇĺek analyzovan√© smńõsi.
F. Zpracování signálu detektoru a ostatních
informací
Zpracování dat a tím kvalitativní i kvantitativní
interpretaci anal√Ĺzy lze prov√©st v jednoduŇ°Ň°√≠m pŇô√≠padńõ zaŇôazen√≠m integr√°toru do
sestavy plynov√©ho chromatografu, ńćastńõjŇ°√≠m vybaven√≠m je vŇ°ak v souńćasn√© dobńõ
jiŇĺ ovl√°d√°n√≠ chromatografick√©ho syst√©mu pońć√≠tańćem. Softwarov√© vybaven√≠ obvykle
registruje vŇ°echny pracovn√≠ podm√≠nky (teplotn√≠ reŇĺim, regulace tlaku a
prŇĮtoku), eviduje poŇôad√≠ anal√Ĺz, pońćet opakov√°n√≠, mńõŇô√≠ eluńćn√≠ ńćasy a plochy
p√≠kŇĮ jednotliv√Ĺch sloŇĺek vzorku, koriguje nulovou linii, ŇôeŇ°√≠ pŇô√≠pady
neoddńõlen√Ĺch l√°tek vytv√°Ňôej√≠c√≠ch sloŇĺen√Ĺ p√≠k apod.
G. PŇô√≠prava vzorkŇĮ
PŇô√≠prava biologick√©ho materi√°lu pŇôed vlastn√≠m proveden√≠m
anal√Ĺzy metodou plynov√© chromatografie odpov√≠d√° sch√©matu popsan√©mu v kapitole
CHROM. Po izolaci, pŇô√≠padnńõ i zakoncentrov√°n√≠ hledan√Ĺch sloŇĺek extrakńćn√≠mi
postupy se zpravidla v plynov√© chromatografii pouŇĺ√≠v√° derivatizańćn√≠ postup. Chemick√°
modifikace umoŇĺŇąuje rychl√Ĺ pŇôechod vzorku do plynn√©ho stavu, zvyŇ°uje
selektivitu, detekovatelnost.
Autorské poznámky
Jaroslava V√°vrov√°