Abstrakt
Technika izoelektrickรฉ fokusace slouลพรญ k separaci lรกtek,
kterรฉ majรญ zรกroveล kyselรฉ i bazickรฉ skupiny. Vyuลพรญvรก se toho, ลพe pลi dosaลพenรญ
izoelektrickรฉho bodu je pohyblivost tฤchto lรกtek nulovรก. Separace probรญhรก na gelech
s vytvoลenรฝm gradientem pH.
Souvisejรญcรญ informace
Elektroforรฉza-v
polyakrylamidovรฉm gelu
Text
Izoelektrickรก fokusace ย (IEF)
Technika izoelektrickรฉ fokusace (izoelektrickรฉho
zaostลovรกnรญ) patลรญ k rovnovรกลพnรฝm technikรกm, kinetickรฝ proces urฤuje pouze
rychlost dosaลพenรญ rovnovรกhy. Pลi separaci ฤรกstic, kterรฉ obsahujรญ zรกroveล kyselรฉ
i basickรฉ skupiny (bรญlkoviny, peptidy, aminokyseliny) je dosaลพenรญm
izoelektrickรฉho bodu pohyblivost iontu nulovรก.
Oblast izoelektrickรฉ fokusace -ย amfolyty
Velmi dลฏleลพitรฝmi slouฤeninami v elektroforรฉze jsou
aminokyseliny. Podle volby pH mohou migrovat jak katodicky tak anodicky, coลพ je
dรกno tรญm, ลพe se jednรก o amfolyty.
Pลรญklad:
b-alaninย ย ย ย ย ย ย ย ย ย rozpuลกtฤn ve vodฤ pลi pH = 7 existuje jakoย ย ย ย "zwitterion"
ย (NH2-CH2-CH2โCOOH)
ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย ย NH3+-CH2-CH2-COO-
Amfolytickรฝ charakter aminokyselin je popsรกn disociaฤnรญmi
konstantami ฤรญslovanรฝmi od kyselรฉ oblasti do zรกsaditรฉ. Disociaฤnรญ konstanta K1
charakterizuje v kyselรฉ oblasti protonizaci karboxylu, tedy proces, kdy se ze
zwitteriontu tvoลรญ kation, druhรก disociaฤnรญ konstanta K2 se vztahuje
k disociaci aminoskupiny, kdy se ze zwitteriontu tvoลรญ anion. Pro b-alanin
jsou hodnoty pK1 = 3,8 a pK2 = 9,6. Iontovรก mobilita
kationtu (pro pH niลพลกรญ neลพ 3,8) je 36 * 10-5 cm2 V-1
s-1 a aniontu (pro pH vyลกลกรญ neลพ 9,6) 31 * 10-5 cm2
V-1 s-1. Je zลejmรฉ, ลพe aminokyseliny typu
mono-amino-mono-karboxy v kyselรฉm prostลedรญ migrujรญ katodicky (jako kationty) a
v zรกsaditรฉm prostลedรญ migrujรญ anodicky. Oblast prakticky nulovรฉ mobility (v
uvedenรฉm pลรญkladu pro pH 6 - 8) je oblastรญ izoelektrickรฉ fokusace.
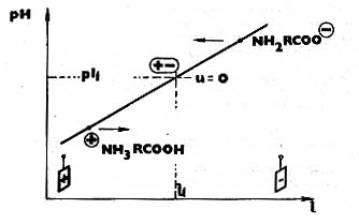
V oblasti pH = pI (pI = izoelektrickรฝ bod
) se separace zastavรญ, s ฤasem se zaostลujรญ zรณny, migrace pลฏsobรญ proti difuzi.
Izoelektrickรก fokusace ve stacionรกrnรญmย pH gradientuย
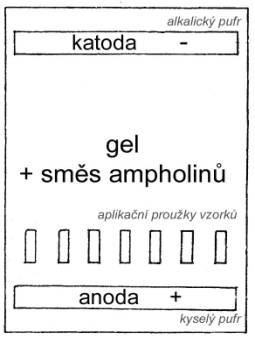
Pลฏsobenรญm elektrickรฉho proudu je vytvoลen podรฉl migraฤnรญ
drรกhy v separaฤnรญm loลพi stacionรกrnรญ pH gradient a amfolyty dรกvkovanรฉ do
libovolnรฉho mรญsta migraฤnรญ drรกhy se pohybujรญ smฤrem k tรฉ oblasti pH, kde jsou
izoelektrickรฉ a stanou se z makroskopickรฉho hlediska nepohyblivรฉ. Vรฝsledkem
analรฝzy je vytvoลenรญ sรฉrie zรณn izoelektrickรฉ spektrum, kterรฉ je stacionรกrnรญ
podรฉl separaฤnรญho loลพe.
Vytvoลenรญย KEY-SpH gradientu
Nejฤastฤji je pouลพรญvรกn zpลฏsob tzv. pลirozenรฉho gradientu
pH. Gradient je tvoลen elektrolรฝzou smฤsi amfoternรญch lรกtek. Vytvoลรญ se
kvazistacionรกrnรญ stav, v nฤmลพ se amfolyty uspoลรกdajรญ podle rostoucรญ hodnoty
izoelektrickรฉho bodu pI od nejniลพลกรญ hodnoty u anody (v elektrodovรฉ komoลe je
silnรก kyselina) k nejvyลกลกรญ hodnotฤ poblรญลพ katody (v elektrodovรฉ komoลe je silnรก
bรกze). Syntetickรฉ smฤsi amfoternรญch lรกtek (ampholiny) jsou alifatickรฉ
polyaminopolykarboxylovรฉ slouฤeniny s molekulovou hmotnostรญ 300ย - 1000 a s pI od 3 do 10. Jde o lรกtky
pลipravenรฉ kondenzacรญ polyethylenaminลฏ s kyselinou akrylovou.
|
|
Izoelektrickรก fokusace se provรกdรญ vฤtลกinou v
polyakrylamidovรฉm gelu v tenkรฝch vrstvรกch a uลพรญvajรญ se pro ni stejnรก zaลรญzenรญ
jako pro zรณnovou elektroforรฉzu. Pracovnรญ postup zahrnuje prefokusaci (bez
vzorku), kdy se vytvรกลรญ gradient pH, a nรกslednou analytickou fokusaci se
vzorkem. Pro IEF lze pouลพรญt jako vhodnรฝ nosiฤ takรฉ agarรณzu,
kterรก mรก nulovou elektroosmรณzu. Jejรญ vรฝhodou je snadnรก pลรญprava gelu a
zdravotnรญ nezรกvadnost. |
Analytickรฉ vyuลพitรญ izoelektrickรฉ fokusace je velmi rozsรกhlรฉ
a leลพรญ pลedevลกรญm v oblastech proteinลฏ (proteiny jsou amfolyty).
Poznรกmky
Appendixy
Literatura
Autorskรฉ poznรกmky
Jaroslava Vรกvrovรก