Abstrakt
 Izoleucin pat┼Ö├Ł mezi
esenci├Īln├Ł glukoplastick├® i ketoplastick├® aminokyseliny. M├Ī podobn├® vlastnosti
jako ostatn├Ł aminokyseliny s rozv─øtven├Įm uhl├Łkat├Įm ┼Öet─øzcem (leucin,
valin) a je nepostradateln├Į pro lidsk├Į organismus. V├Įznamn├Ī je degradace
izoleucinu, kdy vznikaj├Ł mastn├® kyseliny, kter├® se metabolizuj├Ł r┼»zn├Įm
způsobem.
Izoleucin pat┼Ö├Ł mezi
esenci├Īln├Ł glukoplastick├® i ketoplastick├® aminokyseliny. M├Ī podobn├® vlastnosti
jako ostatn├Ł aminokyseliny s rozv─øtven├Įm uhl├Łkat├Įm ┼Öet─øzcem (leucin,
valin) a je nepostradateln├Į pro lidsk├Į organismus. V├Įznamn├Ī je degradace
izoleucinu, kdy vznikaj├Ł mastn├® kyseliny, kter├® se metabolizuj├Ł r┼»zn├Įm
způsobem.
Terminologie
Izoleucin, 2-amino-3-metylvaler├Īt
Synonyma
2-amino-3-metylvaler├Īt, isoleucin
Klasifika─Źn├Ł k├│dy
Odkazy na jin├® relevantn├Ł
dokumenty, dal┼Ī├Ł informace
D─ødi─Źn├®
metabolick├® poruchy aminokyseliny
Chemick├Ī a fyzik├Īln├Ł
charakteristika, struktura a povaha analytu
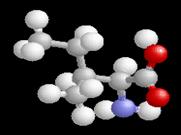
Izoleucin (Ile), NH2CH(CH(CH3)CH2CH3)COOH,
C6H13O2N
m.h. 131,1
Kysel├Ī disocia─Źn├Ł konstanta pK (25 oC)
2,26; 9,62
Izoelektrick├Į bod pI 5,94
Izoleucin je esenci├Īln├Ł aminokyselina, tzn. nelze
ji v organizmu syntetizovat, mus├Ł se z├Łskat potravou nebo ┼Īt─øpen├Łm
tk├Ī┼łov├Įch b├Łlkovin. Podle chemick├®ho charakteru jej├Łho postrann├Łho ┼Öet─øzce ji
┼Öad├Łme mezi nepol├Īrn├Ł, neutr├Īln├Ł a alifatick├® aminokyseliny. Postrann├Ł ┼Öet─øzec
se uplat┼łuje v hydrofobn├Łch interakc├Łch b├Łlkovin.
Izoleucin obsahuje asymetrick├Į atom uhl├Łku nejen
ve hlavn├Łm, ale i postrann├Łm ┼Öet─øzci, tzn. existuje ve ─Źty┼Öech mo┼Šn├Įch
stereoizomern├Łch form├Īch.
Role v metabolismu
M├Ī podobn├® vlastnosti jako ostatn├Ł aminokyseliny
s rozv─øtven├Įm uhl├Łkat├Įm ┼Öet─øzcem (leucin, valin) a je nepostradateln├Į pro
lidsk├Į organismus. V─øt┼Īina aminokyselin ob├Łhaj├Łc├Łch v krvi se metabolizuj├Ł
v j├Ītrech, izoleucin spolu s leucinem a valinem tvo┼Ö├Ł v├Įjimku ŌĆō
proch├Īzej├Ł j├Ītry nezm─øn─øny. Zachycuj├Ł je p┼Öedev┼Ī├Łm mozek a svaly, v nich┼Š
se odbour├Īvaj├Ł.
Zdroj (synt├®za,
p┼Ö├Łjem)
Izoleucin pat┼Ö├Ł mezi esenci├Īln├Ł aminokyseliny,
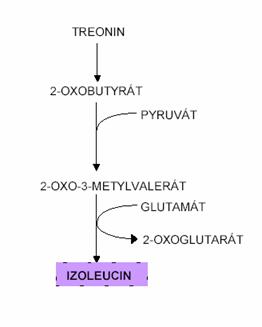
nelze ji tedy v organizmu syntetizovat. Jej├Ł biosynt├®za prob├Łh├Ī vesm─øs jen
u rostlin a mikroorganism┼» a je spole─Źn├Ī pro izoleucin a valin ŌĆō je
katalyzov├Īna stejn├Įmi enzymy. Na 2-oxobutyr├Īt jsou nav├Īz├Īny aktivn├Ł
acetaldehydov├® skupiny, kter├® poch├Īzej├Ł z a-hydroxy-ethylthiamindifosf├Ītu
vznikl├®ho z pyruv├Ītu. Produktem je 2-oxo-3-metylvaler├Īt, z kter├®ho je
p┼Ö├Łmo syntetizov├Īn izoleucin.
Pr┼»myslov─ø je izoleucin (stejn─ø jako v─øt┼Īina
aminokyselin) vyr├Īb─øn biosynt├®zou u┼Šit├Łm mikroorganism┼» nebo chemickou synt├®zou
nebo kombinac├Ł chemick├® synt├®zy a r┼»zn├Įch biotechnologick├Įch postup┼». Je
pou┼Š├Łv├Īn jako sou─Ź├Īst├Ł krmiv pro u┼Šitkov├Ī zv├Ł┼Öata, ochucovadlo potravin,
konzerva─Źn├Ł a antioxida─Źn├Ł p┼Ö├Łpravky.
Distribuce v
organismu, obsah ve tk├Īn├Łch
L-Izoleucin ( OMIM 238340) je ubikvitern├Ł aminokyselina p┼Ö├Łtomn├Ī ve v┼Īech
t─øln├Łch tekutin├Īch, patologicky zv├Į┼Īen├® hladiny v krvi jsou zaznamen├Īny p┼Öedev┼Ī├Łm u choroby javorov├®ho sirupu (OMIM 248600) neboli
leucin├│zy.
Zv├Į┼Īen├® hladiny
izoleucinu jsou zaznamen├Īny tak├® v katabolick├® f├Īzi v├Į┼Šivy, p┼Öi malnutrici,
sepsi, ┼Īoku, komatu a metabolick├® dysbalanci. Pokles hladin izoleucinu v
pr┼»b─øhu parenter├Īln├Ł l├®─Źby je dokladem ├║sp─ø┼Īn├® reutilizace a ├║stupu
katabolismu.
Poruchy metabolismu valinu a
izoleucinu.
Zp┼»sob vylu─Źov├Īn├Ł nebo
metabolismusOSN-E
Izoleucin pat┼Ö├Ł mezi ketoplastick├® i
glukoplastick├® aminokyseliny. Odbour├Īv├Īn├Ł izoleucinu je sled n─økolika reakc├Ł.
Izoleucin je nejprve transaminac├Ł p┼Öem─øn─øn na 2-oxo-3-metylvaler├Īt, kter├Į je
oxida─Źn├Ł dekarboxylac├Ł p┼Öem─øn─øn na 2-metylbutyrylkoenzym A, d├Īle na
2-metylkrotonylkoenzym A a dal┼Ī├Ł odbour├Īv├Īn├Ł prob├Łh├Ī podle sch├®matu b-oxidace. Posledn├Łm krokem je ┼Īt─øpen├Ł
propionylkoenzymu A na sukcinylkoenzym A (sukcinylCoA)
a acetylkoenzym A (acetylCoA). SukcinylCoA vstupuje do citr├Ītov├®ho cyklu jako
kone─Źn├Į produkt odbour├Īv├Īn├Ł izoleucinu a z acetylCoA jsou syntetizov├Īny mastn├®
kyseliny.
Literatura
Z.Vodr├Ī┼Ška: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie.
Academia, Praha 1987.
Autorsk├® pozn├Īmky
Karol├Łna Pe┼Īkov├Ī
recenzoval Viktor Ko┼Šich