Abstrakt
Methionin pat┼Ö├Ł mezi z├Īkladn├Ł esenci├Īln├Ł glukoplastick├® aminokyseliny. Je
hlavn├Łm zdrojem metylov├Įch skupin p┼Öedev┼Ī├Łm pro synt├®zu cholin┼», kreatininu a
adrenalinu v organismu. Adenozylmethionin (metabolicky aktivn├Ł forma
methioninu) je tak├® v├Įznamn├Įm donorem metylov├Įch skupin a p┼»sob├Ł jako koenzym
metyltransfer├Īz. D├Īle je
inhibitorem methylentetrahydrofol├Īt redukt├Īzy (MTHFR) a aktiv├Ītorem
cystathionin-beta-synt├Īzy (CBS).
Terminologie
Methionin, 2-amino-4-(metylthio)butyr├Īt
Synonyma
2-amino-4-(metylthio)butyr├Īt
Odkazy na jin├®
relevantn├Ł dokumenty, dal┼Ī├Ł informace
D─ødi─Źn├®
metabolick├® poruchy aminokyselin
Adenosylhomocystein
Chemick├Ī a fyzik├Īln├Ł
charakteristika, struktura a povaha analytu
Methionin (Met), NH2CH(CH2CH2SCH3)COOH,
C5H11O2SN
m.h. 149,2
Kysel├Ī disocia─Źn├Ł konstanta pK (25 oC)
2,28; 9,21
Izoelektrick├Į bod pI 5,74
Methionin je esenci├Īln├Ł aminokyselina, tzn. nelze
ji v organizmu syntetizovat, mus├Ł se z├Łskat potravou nebo ┼Īt─øpen├Łm
tk├Ī┼łov├Įch b├Łlkovin. Jej├Ł postrann├Ł ┼Öet─øzec m├Ī do zna─Źn├® m├Łry hydrofobn├Ł
charakter (uplat┼łuje se v hydrofobn├Łch interakc├Łch b├Łlkovin), methionin
┼Öad├Łme tedy mezi nepol├Īrn├Ł aminokyseliny. Obsahuje lehce polarizovateln├Į atom
s├Łry, na kter├Į se v├Ī┼Še adenozyl (z ATP) za vzniku adenozylmethioninu.
Methionin obsahuje asymetrick├Į atom uhl├Łku,
existuje proto ve dvou enantiomern├Łch konfigurac├Łch ŌĆō D a L, v b├Łlkovin├Īch
se vyskytuj├Ł pouze L-formy.
Role v metabolismu
Methionin je
hlavn├Łm zdrojem metylov├Įch skupin v organismu, p┼Öedev┼Ī├Łm pro synt├®zu cholin┼»,
kreatinu, methylnikotinamidu a adrenalinu. S-adenozylmethionin (metabolicky
aktivn├Ł forma methioninu) nav├Łc p┼»sob├Ł jako koenzym metyltransfer├Īz, kter├®
katalyzuj├Ł p┼Öenos metylov├® skupiny na r┼»zn├® akceptory.
Zdroj (synt├®za,
p┼Ö├Łjem)
Methionin pat┼Ö├Ł mezi esenci├Īln├Ł aminokyseliny,
nelze ji tedy v organizmu syntetizovat, jej├Ł biosynt├®za prob├Łh├Ī vesm─øs jen
u rostlin a mikroorganism┼». Prekurzorem synt├®zy methioninu je aspart├Īt,
z aspart├Ītu vznik├Ī homoserin, kter├Į reaguje se sukcinylkoenzymem A a
cysteinem za vzniku cystathionu. Ten je hydrolyticky ┼Īt─øpen na homocystein a
pyruv├Īt. Homocystein je metylov├Īn na methionin.
Pr┼»myslov─ø je methionin vyr├Īb─øn chemickou
synt├®zou, kdy je v├Įchoz├Ł surovinou propylen. Je pou┼Š├Łv├Īn p┼Öedev┼Ī├Łm jako p┼Ö├Łsada
do krmiv pro u┼Šitkov├Ī zv├Ł┼Öata.
┬Ā
Distribuce v
organismu, obsah ve tk├Īn├Łch
Methionin (OMIM 250850) je ubikvitern├Ł aminokyselina v┼Īech tk├Īn├Ł a
tekutin.
Patologicky zv├Į┼Īen├®
hladiny v krvi jsou zaznamen├Īny u ┼Öady d─ødi─Źn├Įch poruch metabolismu sirn├Įch
aminokyselin, jako
nap┼Ö. u homocystinurie z deficitu cystationin beta-synt├Īzy. Velmi v├Įrazn├®
zv├Į┼Īen├® hladiny methioninu lze nal├®zt u deficitu methioninadenozyltransfer├Īzy. U remetyla─Źn├Łch poruch b├Įvaj├Ł hladiny
methioninu sn├Ł┼Šen├® ─Źi norm├Īln├Ł a
hladiny cystathioninu v├Įrazn─ø zv├Į┼Īen├®.
Sekund├Īrn─ø m┼»┼Še doj├Łt ke zv├Į┼Īen├Ł hladiny homocysteinu v mo─Źi p┼Öi deficitu
vitam├Łnu B12. Zv├Į┼Īen├Ī
koncentrace fol├Īt┼» zase inhibuje transmetyla─Źn├Ł reakci, kter├Ī vede ke zv├Į┼Īen├®
hladin─ø S-adenosyl-methioninu .
Poruchy metabolismu sirn├Įch AMK.
Zp┼»sob vylu─Źov├Īn├Ł nebo
metabolismusOSN-E
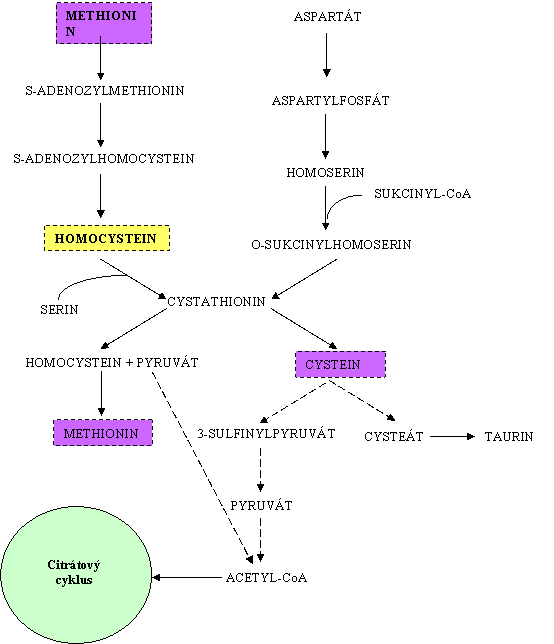
Methionin pat┼Ö├Ł
mezi glukoplastick├® aminokyseliny. Odbour├Īv├Īn├Ł methioninu prob├Łh├Ī takto: methionin je p┼Öem─øn─øn na homocystein (50%
dostupn├®ho homocysteinu je recyklov├Īno zp─øt na methionin). Homocystein m┼»┼Še b├Įt
tak├® slou─Źen se serinem a vytvo┼Öit cystathionin (za p┼Ö├Łtomnosti
pyridoxalfosf├Ītu). Cystathionin je deaminov├Īn a ┼Īt─øpen na cystein a
2-oxobutyr├Īt. Cystein je odbour├Īn p┼Ö├Łmo na pyruv├Īt, ten je oxida─Źn├Ł
dekarboxylac├Ł p┼Öem─øn─øn na acetylkoenzym A (acetylCoA). AcetylCoA vstupuje do
citr├Ītov├®ho cyklu jako kone─Źn├Į produkt odbour├Īv├Īn├Ł methioninu.
Literatura
Z.Vodr├Ī┼Ška: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie.
Academia, Praha 1987.
Autorsk├® pozn├Īmky
Karol├Łna Pe┼Īkov├Ī
recenzoval Viktor Ko┼Šich