Abstrakt
Fenylalanin patéûÙ mezi esenciûÀlnûÙ glukoplastickûˋ i
ketoplastickûˋ aminokyseliny. Fenylalanin je prekurzorem pro biosyntûˋzu hormoné₤
adrenalinu, thyroxinu a trijodthyroninu. Polovina fenylalaninu péijatûˋho
potravou je metabolizovûÀna na tyrozin a druhûÀ polovina, nezbytnûÀ pro ré₤st, je
syntetizovûÀna na bûÙlkovinu.
Terminologie
Fenylalanin, 2-amino-3-fenylpropionûÀt
Synonyma
2-amino-3-fenylpropionûÀt
Odkazy na jinûˋ
relevantnûÙ dokumenty, daléÀûÙ informace
Dádiánûˋ
metabolickûˋ poruchy aminokyselin
ChemickûÀ a fyzikûÀlnûÙ
charakteristika, struktura a povaha analytu
Fenylalanin (Phe), NH2CH(CH2C6H5)COOH,
C9H11O2N
m.h. 165,2
KyselûÀ disociaánûÙ konstanta pK (25 oC)
1,83; 9,13
Izoelektrickû§ bod pI 5,48
Fenylalanin je esenciûÀlnûÙ aminokyselina, tzn.
nelze ji v organizmu syntetizovat, musûÙ se zûÙskat potravou nebo éÀtápenûÙm
tkûÀéovû§ch bûÙlkovin. Podle chemickûˋho charakteru jejûÙho postrannûÙho éetázce ji éadûÙme
mezi nepolûÀrnûÙ aminokyseliny. PostrannûÙ éetázec se uplatéuje
v hydrofobnûÙch interakcûÙch bûÙlkovin.
Aromatickû§ kruh fenylalaninu funguje jako
chromofor a absorbuje ultrafialovûˋ zûÀéenûÙ v oblasti vlnovû§ch dûˋlek 260-300
nm.
Fenylalanin obsahuje asymetrickû§ atom uhlûÙku,
existuje proto ve dvou enantiomernûÙch konfiguracûÙch - D a L, v bûÙlkovinûÀch
se vyskytujûÙ pouze L-formy.
Role v metabolismu
Fenylalanin je spolu s tyrozinem prekurzorem
pro biosyntûˋzu hormoné₤ adrenalinu (déeé nadledvin), thyroxinu a trijodthyroninu
(éÀtûÙtnûÀ éƒlûÀza), dûÀle pro biosyntûˋzu melaniné₤ (pigmenté₤ ké₤éƒe, vlasé₤, vousé₤,
oáûÙ). Polovina fenylalaninu péijatûˋho potravou je metabolizovûÀna na tyrozin a
druhûÀ polovina, nezbytnûÀ pro ré₤st, je syntetizovûÀna na bûÙlkovinu.
Zdroj (syntûˋza,
péûÙjem)
Fenylalanin patéûÙ mezi esenciûÀlnûÙ aminokyseliny,
nelze ji tedy v organizmu syntetizovat. JejûÙ biosyntûˋza probûÙhûÀ vesmás jen
u rostlin a mikroorganismé₤ a je spoleánûÀ pro véÀechny aromatickûˋ aminokyseliny.
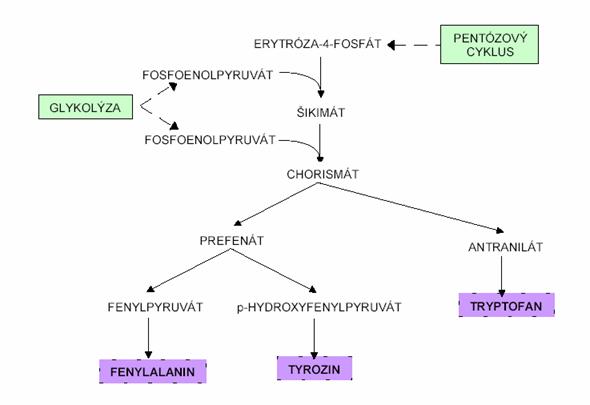
Biosyntûˋza aromatickû§ch aminokyselin zaáûÙnûÀ kondenzacûÙ fosfoenolpryruvûÀtu
(meziprodukt glykolû§zy)
a erytrû°za-4-fosfûÀtu (meziprodukt regeneraánûÙ fûÀze pentû°zovûˋho cyklu). DûÀle pées éadu
meziprodukté₤ vznikûÀ éÀikimûÀt, kterû§ reaguje s daléÀûÙm fosfoenolpyruvûÀtem na
chorismûÀt. Zde se cesta biosyntûˋzy aromatickû§ch aminokyselin vátvûÙ, biosyntûˋza
fenylalaninu probûÙhûÀ nûÀsledovná: z chorismûÀtu vznikûÀ prefenûÀt, dûÀle fenylpyruvûÀt
a z fenylpyruvûÀtu vznikûÀ fenylalanin.
Pré₤myslová je fenylalanin (stejná jako vátéÀina
aminokyselin) vyrûÀbán biosyntûˋzou uéƒitûÙm mikroorganismé₤ nebo chemickou syntûˋzou
nebo kombinacûÙ chemickûˋ syntûˋzy a ré₤znû§ch biotechnologickû§ch postupé₤. Je
pouéƒûÙvûÀn jako souáûÀstûÙ krmiv pro uéƒitkovûÀ zvûÙéata, ochucovadlo potravin,
konzervaánûÙ a antioxidaánûÙ péûÙpravky.
Distribuce v
organismu, obsah ve tkûÀnûÙch
Fenylalanin je esenciûÀlnûÙ aminokyselina s
ubikviternûÙm vû§skytem. Vû§razná zvû§éÀenûˋ hladiny lze nalûˋzt ve véÀech tálesnû§ch
tekutinûÀch péi hyperfenylalaninûˋmii a
klasickûˋ fenylketonurii (OMIM
264070). MûÙrná zvû§éÀenûˋ hladiny v krvi se vyskytujûÙ péi
primapterinurii.
Poruchy metabolismu fenylalaninu.
Zpé₤sob vyluáovûÀnûÙ nebo
metabolismusOSN-E
Fenylalanin patéûÙ mezi glukoplastickûˋ a
ketoplastickûˋ aminokyseliny. HlavnûÙ cesta odbourûÀvûÀnûÙ fenylalaninu je jeho
hydroxylace na tyrozin za katalû§zy fenylalaninhydroxylûÀzy. OdbourûÀvûÀnûÙ
pokraáuje sloéƒitû§m nákolikastupéovû§m procesem: tyrozin je transaminovûÀn na
4-hydroxyfenylpyruvûÀt, ze kterûˋho pées nákolik meziprodukté₤ vznikûÀ
4-fumarylacetoacetûÀt. Z 4-fumarylacetoacetûÀtu je odéÀtápen fumarûÀt, kterû§
vstupuje do citrûÀtovûˋho cyklu a ze zbylûˋho acetoacetûÀtu mohou bû§t syntetizovûÀny
mastnûˋ kyseliny.
VedlejéÀûÙ cesty odbourûÀvûÀnûÙ fenylalaninu, napé.
transaminace na fenylpyrohroznan, jsou pouéƒity ve vátéÀûÙ mûÙée jen péi hromadánûÙ
fenylalaninu v organismu za patologickû§ch podmûÙnek.
Literatura
Z.VodrûÀéƒka: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie.
Academia, Praha 1987.
Autorskûˋ poznûÀmky
KarolûÙna PeéÀkovûÀ
recenze Viktor Koéƒich