Abstrakt
IgG je jedna ze tŇô√≠d imunoglobulinŇĮ, √ļńćastn√≠ se vŇ°ech typŇĮ imunn√≠ch reakc√≠, aktivuje komplement, jeho Mr je 150 kDa.¬† Sledov√°n√≠ hladin IgG m√° v√Ĺznam hlavnńõ u diagnostiky imunodeficienc√≠ a substituńćn√≠ terapie imunoglobuliny.
Terminologie
Synonyma
Klasifikańćn√≠ k√≥dy
Odkazy na jin√© relevantn√≠ dokumenty, dalŇ°√≠ informace
Chemická a fyzikální charakteristika, struktura a povaha analytuOSN-E
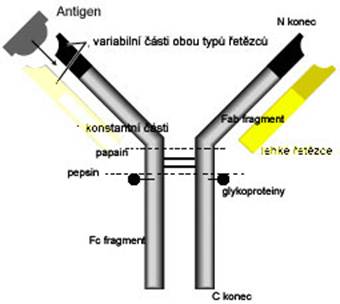
modifikovan√Ĺ obr√°zek z webu
Imunoglobuliny v z√°kladn√≠ struktuŇôe maj√≠ dva identick√© tńõŇĺk√© Ňôetńõzce (H) s molekulovou hmotnost√≠ 50 kDa a dva lehk√© Ňôetńõzce (L) okolo 22 kDa. Ňėetńõzce jsou k sobńõ pout√°ny rŇĮzn√Ĺm pońćtem disulfidick√Ĺch vazeb. H a L Ňôezce jsou tvoŇôeny ńć√°st√≠ variabiln√≠ (V) a konstantn√≠ (C). TńõŇĺk√© i lehk√© Ňôetńõzce maj√≠ vedle sebe spoleńćnńõ N-termin√°ln√≠ konce, skl√°daj√≠ se ze s√©rie globul√°rn√≠ch oblast√≠ z v√Ĺznamn√Ĺch homologn√≠ch aminokyselinov√Ĺch sekvenc√≠ (AMK) oznańćovan√Ĺch jako dom√©ny. N-termin√°ln√≠ dom√©ny
H a L ŇôetńõzcŇĮ obsahuj√≠ variabiln√≠ aminokyselinov√© sekvence (V oblast), kter√© determinuj√≠ antigenn√≠ specifitu. N-termin√°ln√≠ AMK ve V oblasti formuj√≠ funkńćn√≠ region, kam se usad√≠ antigenn√≠ epitop. Povrchy vazebn√Ĺch m√≠st a epitopŇĮ jsou navz√°jem komplement√°rn√≠ a podle struktury, v√ĹbńõŇĺkŇĮ, se pr√°vńõ jedinńõ ten spr√°vn√Ĺ epitop ze vŇ°ech nav√°Ňĺe na patŇôińćn√© vazebn√© m√≠sto. Komplementarita nen√≠ pouze struktur√°ln√≠, ale i chemick√° a to na podkladńõ van der Waalsov√Ĺch sil. Jedn√° se o vod√≠kov√© vazby mezi pol√°rn√≠mi skupinami, o vytvoŇôen√≠ iontov√Ĺch vazeb mezi rŇĮznńõ nabit√Ĺmi stranami ŇôetńõzcŇĮ. Mezi V oblast√≠ a zb√Ĺvaj√≠c√≠ ńć√°st√≠ konstantn√≠ho H Ňôetńõzce (CH) jsou strukturn√≠ a antigenn√≠ rozd√≠ly, kter√© imunoglobuliny rozdńõluj√≠ do podtŇô√≠d. NapŇô√≠klad u IgG molekul CH dom√©ny maj√≠ n√°sleduj√≠c√≠ funkce: prvn√≠ (CH1) a druh√° (CH2) dom√©na formuj√≠ ‚Äěskryt√© m√≠sto‚Äú, kter√© odpov√≠d√° za transformaci z T formy (v roztoku) do V formy pŇôi nav√°z√°n√≠ antigenu. CH1 dom√©na se v√°Ňĺe na sloŇĺky komplementu C1q, kter√© vedou k aktivaci klasick√© cesty kask√°dy komplement√°rn√≠ho syst√©mu. TŇôet√≠ dom√©na (CH3) zprostŇôedkov√°v√° vazbu Fc fragmentu na¬† Fc receptor bunńõk imunitn√≠ho syst√©mu -granulocyty, monocyty, makrof√°gy. Kombinace CH2 a CH3 spoleńćnńõ tvoŇô√≠ dalŇ°√≠ dom√©nu pro vazbu napŇô. granulocytŇĮ a NK (natural killers) bunńõk.
Papain Ň°tńõp√≠ molekulu imunoglubulinu na tŇôi ńć√°sti, dva identick√© Fab fragmenty sest√°vaj√≠c√≠ z kompletn√≠ch L ŇôetńõzcŇĮ (V oblast) a ńć√°sti konstantn√≠ch H ŇôetńõzcŇĮ. Zb√Ĺvaj√≠c√≠ segment z konstantn√≠ch oblast√≠ dvou tńõŇĺk√Ĺch ŇôetńõzcŇĮ spojen√Ĺch disulfidick√Ĺmi mŇĮstky je oznańćov√°n jako Fc fragment (c=crystallizable, krystalizuj√≠c√≠).
Lehk√© Ňôetńõzce jsou typu kappa nebo lambda. KaŇĺd√° molekula m√° dva kappa nebo 2 lambda L Ňôetńõzce, protoŇĺe kaŇĺd√° B buŇąka je schopna produkovat pouze jeden typ lehk√Ĺch ŇôetńõzcŇĮ. Lehk√© Ňôetńõzce maj√≠ N (amino)-termin√°ln√≠, variabiln√≠ a C (karboxy) termin√°ln√≠, konstantn√≠ konce. L Ňôetńõzce jsou pŇôipojeny k H ŇôetńõzcŇĮ prostŇôednictv√≠m disulfidick√Ĺch mŇĮstkŇĮ, kter√© vytv√°Ňô√≠ cystinov√© molekuly mezi konstantn√≠mi oblastmi obou typŇĮ ŇôetńõzcŇĮ. B lymfocyty produkuj√≠ prŇĮmńõrnńõ dvakr√°t v√≠ce kappa ŇôetńõzcŇĮ neŇĺ lambda. Term√≠n monoklon√°ln√≠ lehk√© Ňôetńõzce nebo Bence Jones b√≠lkovina je v podstatńõ dŇĮsledek sekrece malignńõ transformovan√Ĺch a proliferuj√≠c√≠ch bunńõk kmene B lymfocytŇĮ produkuj√≠c√≠ dan√Ĺ typ L ŇôetńõzcŇĮ.
UvolŇąov√°n√≠ L ŇôetńõzcŇĮ z vazby je umoŇĺnńõno sklony cystinov√Ĺch molekul k snadn√© dimerizaci.
Struktura H Ňôetńõzce je dan√° tŇô√≠dou dan√©ho imunoglobulinu. Rozd√≠ly mezi imunoglobulinov√Ĺmi skupinami jsou v jejich aminokyselinov√©m sloŇĺen√≠, sekvenci, molekulov√© hmotnosti, v sacharidov√Ĺch zbytc√≠ch, antigenitńõ, alotypov√© heterogenitńõ a elektroforetick√© mobilitńõ. Je 5 z√°kladn√≠ skupin tńõŇĺk√Ĺch ŇôetńõzcŇĮ, kaŇĺd√° m√° dva identick√© Ňôetńõzce, IgG skupina m√° dva γ (gama) tńõŇĺk√© Ňôetńõzce, IgA m√° α (alfa) Ňôetńõzce, IgM m√° ¬Ķ (m√≠) Ňôetńõzce, IgD-δ (delta) Ňôetńõzce, IgE ε (epsilon) dva tńõŇĺk√© Ňôetńõzce.
J Ňôetńõzce jsou spojky mezi samotn√Ĺmi molekulami globulinŇĮ. Imunoglobuliny tŇô√≠dy IgM a IgA vykazuj√≠ polymorfismy. IgM molekuly se vyskytuj√≠c√≠ zejm√©na jako pentametry, IgA jako dimer. IgM monomery stejnńõ tak jako IgA monomery jsou spojeny pr√°vńõ prostŇôednictv√≠m J ŇôetńõzcŇĮ. J Ňôetńõzce jsou glykoproteiny o molekulov√© hmotnosti 15 kDa a cestou disulfidick√Ĺch vazeb pobl√≠Ňĺ C termin√°ln√≠ch koncŇĮ spojuj√≠ mezi sebou tńõŇĺk√© Ňôetńõzce imunoglobulinŇĮ.
Sekreńćn√≠ dimery IgA, kter√© jsou produkov√°ny plazmocyty respirańćn√≠ho, urogenit√°ln√≠ho a gastrointestin√°ln√≠ho traktu a uvolŇąov√°ny do tńõln√≠ch tekutin s obsahem sekreńćn√≠ komponenty, kter√° chr√°n√≠ imunoglobuliny pŇôed Ň°tńõp√≠c√≠mi √ļńćinky peptid√°z. Sekreńćn√≠ komponenta je glykoprotein s molekulovou hmotnost√≠ 70 kDa. Dimerick√© molekuly IgA se nenav√°Ňĺou na sekreńćn√≠ komponenty dokud neprojdou epiteli√°ln√≠m povrchem sliznic, kter√© sekreńćn√≠ komponentu syntetizuj√≠. V pŇô√≠padńõ sekreńćn√≠ IgA deficience, je sekreńćn√≠ komponenta stanoviteln√°.
Antigenn√≠ heterogenita se dńõl√≠ na izotypovou, alotypovou, idiotypovou. Izotypy maj√≠ stejn√© konstantn√≠ dom√©ny. Izotypov√© variace maj√≠ odliŇ°nosti v H, L Ňôetńõzc√≠ch, dom√©n√°ch, kter√© jsou prezentov√°ny ve vŇ°ech zdrav√Ĺch jedinc√≠ch dan√©ho druhu. Synt√©za izotopŇĮ je k√≥dov√°na geny pŇô√≠sluŇ°n√©ho jedince a druhu. Alotypov√° variace je definov√°na jako alelou indukovan√° variace imunoglobulinu uvnitŇô druhu. Alotypy se objevuj√≠ jako variace konstantn√≠ ńć√°sti H Ňôetńõzce. Alotypov√© variace jsou ńćasto dŇĮsledek AMK v√Ĺmńõn uvnitŇô H Ňôetńõzce. Idiotypy maj√≠ stejn√© variabiln√≠ dom√©ny. Idiotypov√© variace souvis√≠ s rozmanitost√≠ v antigenn√≠ch vazebn√Ĺch m√≠stech. Imunoglobuliny syntetizovan√© jedn√≠m klonem plazmatick√Ĺch bunńõk jsou norm√°lnńõ kompletnńõ identick√©, vytv√°Ňô√≠ uniformn√≠ idiotyp. Alterace, zmńõny AMK ve V oblasti vytv√°Ňô√≠ idiotypov√© variace. Stejnńõ tak antigeny mŇĮŇĺeme dńõlit na stejn√© izotypy nebo alotypy. V pŇô√≠padńõ paraproteinŇĮ se jedn√° pravdńõpodobnńõ o idiotypovou variaci.
Role v metabolismu
IgM¬† zajiŇ°Ň•uj√≠ ochranu organismu u prim√°rn√≠ch (prim√°rn√≠ protil√°tkou zprostŇôedkovan√° odpovńõńŹ) infekc√≠. IgG jsou sekund√°rn√≠ protil√°tkou u infekc√≠, kter√© jiŇĺ organismus prodńõlal (sekund√°rn√≠ protil√°tkov√° odpovńõńŹ). Zhruba polovina vŇ°ech IgG je v plazmńõ, druh√° polovina je v tńõlesn√Ĺch tekutin√°ch. PŇôi elektroforetick√©m dńõlen√≠ b√≠lkovin s√©ra IgG jsou lokalizov√°ny v gama frakci. Za norm√°ln√≠ch okolnost√≠ IgG2 a IgG4 migruj√≠ spoleńćnńõ k anodńõ a IgG1 a 3 ke katodick√© ńć√°sti gama frakce.¬† Fet√°ln√≠ IgG z mateŇôsk√© krve bńõhem prvn√≠ch 20 gestańćn√≠ch t√ĹdnŇĮ plodu odpov√≠d√° zhruba 10% koncentrace Ig (imunoglobulinu) dospńõl√Ĺch jedincŇĮ. Fet√°ln√≠ infekce bńõhem t√©to periody nevedou ke zv√ĹŇ°en√≠ hladiny Ig. Mezi 22. a 28. gestańćn√≠m t√Ĺdnem vńõku plodu doch√°z√≠ k v√Ĺrazn√©mu zv√ĹŇ°en√≠ placent√°rn√≠ permeability, Ig z mateŇôsk√© krve pŇôech√°z√≠ do plodu a hladina Ig plodu se vyrovn√°v√° hladinńõ Ig matky. Koncentrace IgG1,3,4 jsou stejn√© u plodu jako matky zat√≠mco IG2 je niŇĺŇ°√≠. Po obdrŇĺen√≠ matern√°ln√≠ch imunoglobulinŇĮ se zvyŇ°uje cirkulace v plodu s polońćasem 30 dn√≠. Tato koncentrace pŇôetrv√°v√° aŇĺ do 3 aŇĺ 4 mńõs√≠ce po porodu (3,5-4 g/l). NeŇĺ synt√©zu Ig zcela samostatnńõ pŇôevezme novorozen√Ĺ organismus pŇôekr√Ĺvaj√≠ se hladiny mateŇôsk√©ho a vlastn√≠ho Ig, kdy koncentrace celkov√©ho Ig u novorozence na konci 1. roku je 7 aŇĺ 8 g/l. Synt√©za IgG je z√°visl√° na vyzr√°v√°n√≠ imunitn√≠ho syst√©mu, vytv√°Ňôen√≠ antigenn√≠ odpovńõdi po pŇôirozen√© expozici antigenŇĮm. Jedn√° se o proteinov√© antigeny (v bakteri√≠ch, virech) vedouc√≠ k IgG1,3 synt√©ze a indukovan√© CD4+ buŇąkami, sacharidov√© antigeny (enkapsulovan√© bakterie jako pneumokokov√© kmeny, streptokoky skupiny A, H, influenza viry) reaguj√≠c√≠ zmnoŇĺen√≠m IgG2 a ńć√°steńćnńõ IgG1 a neindukovan√© CD4+ buŇąkami. Na organismus pŇĮsob√≠ i expozice polyvalentn√≠mi antigeny charakteru parazitŇĮ, hmyzu, had√≠ch jedŇĮ, potravinov√Ĺch alergenŇĮ, kter√© pŇĮsob√≠ jako chronick√° antigenn√≠ stimulace na produkci IgG4. IgG4 protil√°tky stejnńõ jako IgE se v√°Ňĺ√≠ na povrchov√© receptory mastocytŇĮ a stimuluj√≠ tvorbu IgG1 a 3 tvorbu autoprotil√°tek.
Zdroj (synt√©za, pŇô√≠jem)
V s√©ru zdrav√Ĺch jedincŇĮ se nach√°z√≠ vŇ°echny tŇô√≠dy imunoglobulinŇĮ: IgG, IgA, IgM, IgD, IgE ve fyziologick√© koncentraci. IgG m√° 4 podtŇô√≠dy, u IgA a IgM jsou zn√°my dvńõ podtŇô√≠dy.
Distribuce v organismu, obsah ve tkáních
IgG se vyskytuje ve 4 tŇô√≠d√°ch. IgG1 je zastoupeno v 60-75%, IgG2 v 15-25%, IgG3 v 3-6%, IgG4 v 2-6%. Produkce specifick√Ĺch protil√°tek jednotliv√Ĺch tŇô√≠d je z√°visl√° na stimuluj√≠c√≠m antigenu. Analyticky se daj√≠ stanovovat vŇ°echny podtŇô√≠dy IgG.
ZpŇĮsob vyluńćov√°n√≠ nebo metabolismus
Produkce IgG v jednotliv√Ĺch podtŇô√≠d√°ch je regulov√°na interleukiny a ńć√°steńćnńõ urńćov√°na i pońćtem B bunńõńćn√Ĺch subpopulac√≠ v tk√°n√≠ch. NapŇô√≠klad u zdrav√Ĺch jedincŇĮ je dominantn√≠ podtŇô√≠dou IgG 1 a 2 v plazmńõ, v tonzil√°ch dominuj√≠ cytoplazmatick√© buŇąky s produkc√≠ IgG1 a 3. Ve struktuŇôe IgG m√° velk√Ĺ v√Ĺznam Fc fragment, kter√Ĺ umoŇĺŇąuje vazbu na Fc receptory bunńõk imunitn√≠ho syst√©mu. Odpov√≠d√° za vychyt√°v√°n√≠ bakteri√≠ makrof√°gy, kter√© jsou atakov√°ny IgG molekulami, kdy Fc fragment IgG se nav√°Ňĺe na Fc receptor makrof√°gŇĮ a nav√°zan√© bakterie na Ig jsou obalov√°ny a nakonec inkorporov√°ny do makrof√°gŇĮ k destrukci. Mezi buŇąky s Fc receptory patŇô√≠ i monocyty, granulocyty, lymfocyty. Katabolismus IgG z√°vis√≠ na jeho plazmatick√© hladinńõ. PŇôi vyŇ°Ň°√≠ch hodnot√°ch IgG je clearance zrychlena aŇĺ na polońćas 11 dn√≠, pŇôi n√≠zk√© synt√©ze IgG je polońćas prodlouŇĺen i na 30 dn√≠.
Biologick√Ĺ polońćas
7-21 dní
Kontroln√≠ (Ňô√≠d√≠c√≠) mechanismy
Literatura
Lothar Thomas, Clinical Laboratory Diagnostics, 1st. English Edition, TH-Books, Germany 1998
Pozn√°mky
IgD m√° Mr 175 kDa.
Appendixy
Autorské poznámky
JiŇôina Luk√°Ň°kov√° (2008)