Abstrakt
Methionin
patří mezi základní esenciální glukoplastické aminokyseliny. Je hlavním zdrojem
metylových skupin především pro syntézu cholinů, kreatininu a adrenalinu
v organismu. Adenozylmethionin (metabolicky aktivní forma methioninu) je také
významným donorem metylových skupin a působí jako koenzym metyltransferáz. Dále je inhibitorem methylentetrahydrofolát reduktázy
(MTHFR) a aktivátorem cystathionin-beta-syntázy (CBS).
Terminologie
Methionin, 2-amino-4-(metylthio)butyrát
Synonyma
2-amino-4-(metylthio)butyrát
Odkazy na jiné relevantní
dokumenty, další informace
href="HYAAA.htm">Dědičné metabolické
poruchy aminokyselin
href="KPADZ.htm">Adenosylhomocystein
Chemická a fyzikální
charakteristika, struktura a povaha analytu
Methionin (Met), NH2CH(CH2CH2SCH3)COOH,
C5H11O2SN
m.h. 149,2
Kyselá disociační konstanta pK (25 oC)
2,28; 9,21
Izoelektrický bod pI 5,74
Methionin je esenciální aminokyselina, tzn. nelze ji
v organizmu syntetizovat, musí se získat potravou nebo štěpením tkáňových
bílkovin. Její postranní řetězec má do značné míry hydrofobní charakter
(uplatňuje se v hydrofobních interakcích bílkovin), methionin řadíme tedy
mezi nepolární aminokyseliny. Obsahuje lehce polarizovatelný atom síry, na
který se váže adenozyl (z ATP) za vzniku adenozylmethioninu.
Methionin obsahuje asymetrický atom uhlíku, existuje
proto ve dvou enantiomerních konfiguracích – D a L, v bílkovinách se
vyskytují pouze L-formy.
Role v metabolismu
Methionin je hlavním zdrojem metylových skupin
v organismu, především pro syntézu cholinů, kreatininu, methylnikotinamidu
a adrenalinu. Adenozylmethionin (metabolicky aktivní forma methioninu) je také
významným donorem metylových skupin a navíc působí jako koenzym
metyltransferáz, které katalyzují přenos metylové skupiny na různé akceptory.
Zdroj (syntéza, příjem)
Methionin patří mezi esenciální aminokyseliny, nelze ji
tedy v organizmu syntetizovat, její biosyntéza probíhá vesměs jen u
rostlin a mikroorganismů. Prekurzorem syntézy methioninu je aspartát,
z aspartátu vzniká homoserin, který reaguje se sukcinylkoenzymem A a
cysteinem za vzniku cystathionu. Ten je hydrolyticky štěpen na homocystein a
pyruvát. Homocystein je metylován na methionin.
Průmyslově je methionin vyráběn chemickou syntézou, kdy
je výchozí surovinou propylen. Je používán především jako přísada do krmiv pro
užitková zvířata.
Distribuce v organismu, obsah
ve tkáních
Methionin (OMIM 250850) je ubikviterní aminokyselina všech tkání a
tekutin. href="AJEJX.htm">Poruchy metabolismu sirných AMK.
Způsob vylučování nebo metabolismus
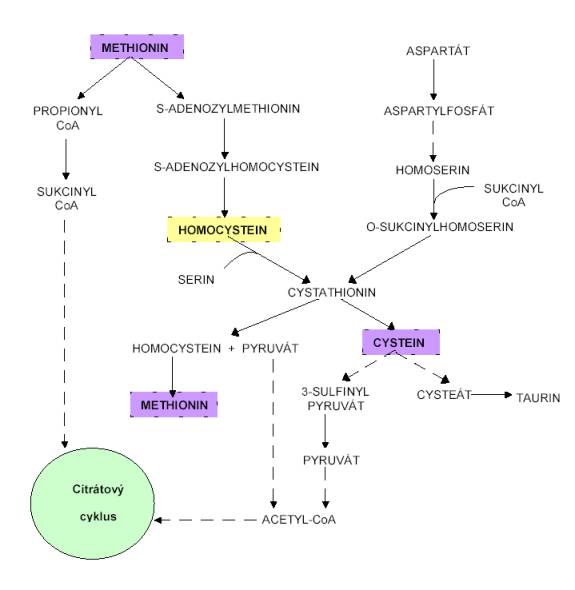
Methionin patří mezi glukoplastické aminokyseliny.
Odbourávání methioninu může probíhat dvěma cestami: jedna cesta je přes
propionylkoenzym A na sukcinylkoenzym A (sukcinylCoA). SukcinylCoA vstupuje do
citrátového cyklu jako konečný produkt odbourávání methioninu.
Druhá
cesta vede přes řadu významných meziproduktů: methionin je hydrolyzován na
homocystein, ten se může opět zpět přeměnit na methionin (remethylace při relativním nedostatku methioninu)
nebo kondenzací homocysteinu se serinem
vzniká cystathionin, který je deaminován na cystein (transulfurace při
nadbytku methioninu). Cystein je odbourán
přímo na pyruvát, ten je oxidační dekarboxylací přeměněn na acetylkoenzym A
(acetylCoA). AcetylCoA vstupuje do citrátového cyklu jako konečný produkt odbourávání
methioninu.
Literatura
Z.Vodrážka: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie. Academia,
Praha 1987.
Autorské poznámky
Karolína Pešková
recenzoval Josef Hyánek