Abstrakt
IgA je jedna ze tříd imunoglobulinů, účastní se hlavně slizniční imunity, jeho Mr je 160 kDa. Sledování hladin IgA má význam hlavně u diagnostiky imunodeficiencí (deficit ve třídě IgA je nejčastější) a substituční terapie imunoglobuliny.
Terminologie
Synonyma
Klasifikační kódy
Odkazy na jiné relevantní dokumenty, další informace
Chemická a fyzikální charakteristika, struktura a povaha analytuOSN-E
Imunoglobuliny v základní struktuře mají dva identické těžké řetězce (H) s molekulovou hmotností 50 kDa a dva lehké řetězce (L) okolo 22 kDa. Řetězce jsou k sobě poutány různým počtem disulfidických vazeb. H a L řezce jsou tvořeny částí variabilní (V) a konstantní (C). Těžké i lehké řetězce mají vedle sebe společně N-terminální konce, skládají se ze série globulárních oblastí z významných homologních aminokyselinových sekvencí (AMK) označovaných jako domény. N-terminální domény H a L řetězců obsahují variabilní aminokyselinové sekvence (V oblast), které determinují antigenní specifitu. N-terminální AMK ve V oblasti formují funkční region, kam se usadí antigenní epitop. Povrchy vazebných míst a epitopů jsou navzájem komplementární a podle struktury, výběžků, se právě jedině ten správný epitop ze všech naváže na patřičné vazebné místo. Komplementarita není pouze strukturální, ale i chemická a to na podkladě van der Waalsových sil. Jedná se o vodíkové vazby mezi polárními skupinami, o vytvoření iontových vazeb mezi různě nabitými stranami řetězců. Mezi V oblastí a zbývající částí konstantního H řetězce (CH) jsou strukturní a antigenní rozdíly, které imunoglobuliny rozdělují do podtříd. Například u IgG molekul CH domény mají následující funkce: první (CH1) a druhá (CH2) doména formují „skryté místo“, které odpovídá za transformaci z T formy (v roztoku) do V formy při navázání antigenu. CH1 doména se váže na složky komplementu C1q, které vedou k aktivaci klasické cesty kaskády komplementárního systému. Třetí doména (CH3) zprostředkovává vazbu Fc fragmentu na Fc receptor buněk imunitního systému -granulocyty, monocyty, makrofágy. Kombinace CH2 a CH3 společně tvoří další doménu pro vazbu např. granulocytů a NK (natural killers) buněk.
Papain štěpí molekulu imunoglubulinu na tři části, dva identické Fab fragmenty sestávající z kompletních L řetězců (V oblast) a části konstantních H řetězců. Zbývající segment z konstantních oblastí dvou těžkých řetězců spojených disulfidickými můstky je označován jako Fc fragment (c=crystallizable, krystalizující).
Lehké řetězce jsou typu kappa nebo lambda. Každá molekula má dva kappa nebo 2 lambda L řetězce, protože každá B buňka je schopna produkovat pouze jeden typ lehkých řetězců. Lehké řetězce mají N (amino)-terminální, variabilní a C (karboxy) terminální, konstantní konce. L řetězce jsou připojeny k H řetězců prostřednictvím disulfidických můstků, které vytváří cystinové molekuly mezi konstantními oblastmi obou typů řetězců. B lymfocyty produkují průměrně dvakrát více kappa řetězců než lambda. Termín monoklonální lehké řetězce nebo Bence Jones bílkovina je v podstatě důsledek sekrece maligně transformovaných a proliferujících buněk kmene B lymfocytů produkující daný typ L řetězců.
Uvolňování L řetězců z vazby je umožněno sklony cystinových molekul k snadné dimerizaci.
Struktura H řetězce je daná třídou daného imunoglobulinu. Rozdíly mezi imunoglobulinovými skupinami jsou v jejich aminokyselinovém složení, sekvenci, molekulové hmotnosti, v sacharidových zbytcích, antigenitě, alotypové heterogenitě a elektroforetické mobilitě. Je 5 základní skupin těžkých řetězců, každá má dva identické řetězce, IgG skupina má dva γ (gama) těžké řetězce, IgA má α (alfa) řetězce, IgM má µ (mí) řetězce, IgD-δ (delta) řetězce, IgE ε (epsilon) dva těžké řetězce.
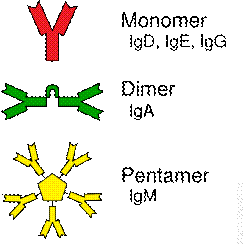
J řetězce jsou spojky mezi samotnými molekulami globulinů. Imunoglobuliny třídy IgM a IgA vykazují polymorfismy. IgM molekuly se vyskytující zejména jako pentametry, IgA jako dimer. IgM monomery stejně tak jako IgA monomery jsou spojeny právě prostřednictvím J řetězců. J řetězce jsou glykoproteiny o molekulové hmotnosti 15 kDa a cestou disulfidických vazeb poblíž C terminálních konců spojují mezi sebou těžké řetězce imunoglobulinů.
Sekreční dimery IgA, které jsou produkovány plazmocyty respiračního, urogenitálního a gastrointestinálního traktu a uvolňovány do tělních tekutin s obsahem sekreční komponenty, která chrání imunoglobuliny před štěpícími účinky peptidáz. Sekreční komponenta je glykoprotein s molekulovou hmotností 70 kDa. Dimerické molekuly IgA se nenavážou na sekreční komponenty dokud neprojdou epiteliálním povrchem sliznic, které sekreční komponentu syntetizují. V případě sekreční IgA deficience je sekreční komponenta stanovitelná.
Antigenní heterogenita se dělí na izotypovou, alotypovou, idiotypovou. Izotypy mají stejné konstantní domény. Izotypové variace mají odlišnosti v H, L řetězcích, doménách, které jsou prezentovány ve všech zdravých jedincích daného druhu. Syntéza izotopů je kódována geny příslušného jedince a druhu. Alotypová variace je definována jako alelou indukovaná variace imunoglobulinu uvnitř druhu. Alotypy se objevují jako variace konstantní části H řetězce. Alotypové variace jsou často důsledek AMK výměn uvnitř H řetězce. Idiotypy mají stejné variabilní domény. Idiotypové variace souvisí s rozmanitostí v antigenních vazebných místech. Imunoglobuliny syntetizované jedním klonem plazmatických buněk jsou normálně kompletně identické, vytváří uniformní idiotyp. Alterace, změny AMK ve V oblasti vytváří idiotypové variace. Stejně tak antigeny můžeme dělit na stejné izotypy nebo alotypy. V případě paraproteinů se jedná pravděpodobně o idiotypovou variaci.
Role v metabolismu
IgA se vyskytuje ve formě sérové nebo sekreční. Strukturálně H řetězce IgA (alfa řetězce) jsou podobné IgG, ale C terminální část má navíc 18 AMK. Předposlední cystin obsahuje vazebné místo pro J řetězec pro polymerizaci IgA.
Sérový IgA je tvořen v 90% monomery, jen z 10% polymery. Sérový IgA má tendenci vytvářet polymerní komplexy, speciálně s albuminem, ale také s enzymy za vzniku makroenzymů. Polovina sérového IgA je lokalizována intravaskulárně. Poměr mezi oběma izotypy IgA1/IgA2 je 9:1. Při sérovém elektroforetickém dělení je IgA lokalizováno do katodické části beta globulinové a anodické oblasti gama globulinové frakce.
Protože IgA neprochází přes placentární bariéru, nevyskytuje se ve fetální krvi. Po narození IgA syntéza začíná pomalu, na konci 1. roku dítěte dosahuje hladina IgA 25% hladiny dospělých. Ve 3,5 letech je hladina asi 50% a v 16 letech dosahuje norem dospělých. Všechny funkce IgA nejsou známy, ale vede alternativní cestou k aktivaci komplementu a má specifické protilátkové funkce. Katabolismus IgA je závislý na jeho sérové hladině.
Sekreční IgA je složen ze dvou molekul spojených J řetězcem a má sekreční komponentu. Sekreční IgA je produkován plazmatickými buňkami v lamina propria mukózní membrány, je syntetizován nezávisle na sérovém IgA, deficit sérového IgA nemusí znamenat deficit sekrečního IgA. Sekreční IgA je zejména Ig tělesných tekutin jako jsou sliny, slzy, kolostrum, nosní sekret, mateřské mléko. Novorozenci a malé děti jsou zásobovány IgA z mateřského mléka, jsou tedy pasivně imunizovány proti gastrointestinálním infekcím. Esenciální funkcí IgA je vazba mikroorganismů k mukózní sliznici, aktivace alternativní cesty komplementu, aktivace zánětlivých reakcí. Uvnitř epiteliálních buněk IgA neutralizuje intracelulární mikroorganismy. V lamina propria mukózní membrány IgA váže antigeny do formy imunokomplexů a sekretuje je na slizniční povrchy. To zabraňuje cirkulaci z nadměrného přetížení imunitními komplexy. Jedinci s deficitem sekrečního IgA jsou postiženy velmi závažnými mukózními, slizničními infekcemi, atopickými a autoimunitními infekcemi.
Zdroj (syntéza, příjem)
V séru zdravých jedinců se nachází všechny třídy imunoglobulinů: IgG, IgA, IgM, IgD, IgE ve fyziologické koncentraci. IgG má 4 podtřídy, u IgA a IgM jsou známy dvě podtřídy.
Distribuce v organismu, obsah ve tkáních
Způsob vylučování nebo metabolismus
Biologický poločas
6 dní
Kontrolní (řídící) mechanismy
Literatura
Lothar Thomas, Clinical Laboratory Diagnostics, 1st. English Edition, TH-Books, Germany 1998
Poznámky
Appendixy
Autorské poznámky
Jiřina Lukášková (2008)