Abstrakt
Chromatografie na pap├¡┼Öe je aplikac├¡ techniky kapalinov├®
chromatografie. Slo┼¥ky na chromatogramu putuj├¡ v podob─ø skvrn, deteguj├¡ se
vhodnou fyzik├íln├¡ nebo chemickou metodou.V├¢hodou plo┼ín├®ho uspo┼Ö├íd├ín├¡ je mo┼¥nost
sou─ìasn├® anal├¢zy libovoln├®ho po─ìtu standard┼» k potvrzen├¡ identity jednotliv├¢ch
komponent.
Související informace
┬À
Chromatografie kapalinová (LC)
┬À
Chromatografie iontov─ø-v├¢m─ønn├í (IEC)
┬À
Chromatorafie tenkovrstvá (TLC)
Text
Chromatografie na papíře
Papírová chromatografie je nejstarší chromatografickou
technikou u┼¥├¡vanou v klinick├® chemii. O jej├¡ v─øhlas se zaslou┼¥ily p┼Öedev┼í├¡m
pr├íce z oblasti anal├¢zy aminokyselin a peptid┼», kter├® umo┼¥nily dal┼í├¡ objevy v
biologii a biochemii. Technika kapalinov├® chromatografie v plo┼ín├®m uspo┼Ö├íd├ín├¡
spo─ì├¡v├í v tom, ┼¥e sorbent m├í podobu tenk├® vrstvy. P┼Öi pap├¡rov├® chromatografii
je touto vrstvou chromatografick├¢ pap├¡r. Princip pap├¡rov├® a tenkovrstv├®
chromatografie spo─ì├¡v├í v tom, ┼¥e p┼Öi pr┼»chodu rozpou┼ít─ødla pap├¡rem nebo vrstvou
dochází k separaci látek. Na chromatografickÛ papír či tenkou vrstvu se vyznačí
ve vhodn├® vzd├ílenosti od okraje start s body pro nanesen├¡ analyzovan├¢ch vzork┼»,
na ozna─ìen├í m├¡sta se nanesou vzorky v kapaln├® form─ø a po odpa┼Öen├¡ rozpou┼ít─ødla
se chromatogram um├¡st├¡ do chromatografick├® komory, kter├í je nasycena parami
stacion├írn├¡ i mobiln├¡ f├íze. Stacion├írn├¡ f├íze je zakotvena v pap├¡┼Öe (vrstv─ø),
mobiln├¡ f├íze prot├®k├í pap├¡rem ─ìi vrstvou vlivem kapil├írn├¡ch sil.
Chromatografick├¢ pap├¡r se bu─Å zav─øs├¡ do lodi─ìky s rozpou┼ít─ødlem a rozpou┼ít─ødlo
prot├®k├í pap├¡rem sestupn─ø, nebo se pap├¡r sto─ìen├¢ do v├ílce ─ìi tenk├í vrstva
sorbentu postav├¡ na dno chromatografick├® komory, v n├¡┼¥ je ji┼¥ p┼Öedem p┼Öipraveno
rozpou┼ít─ødlo (mobiln├¡ f├íze), v tomto p┼Ö├¡pad─ø vlivem kapil├írn├¡ch sil vzl├¡n├í
rozpou┼ít─ødlo po chromatogramu vzh┼»ru a un├í┼í├¡ s sebou jednotliv├® slo┼¥ky, kter├®
se d─øl├¡ na z├íklad─ø sv├¢ch rozpustnost├¡. Tento zp┼»sob se naz├¢v├í vzestupn├®
vyv├¡jen├¡. Vzestupn├® uspo┼Ö├íd├ín├¡ je obvyklej┼í├¡ u tenkovrstv├® chromatografie. Dos├íhne-li ─ìelo mobiln├¡ f├íze
dostate─ìn├® vzd├ílenosti, ozna─ì├¡ se a chromatogram se vyjme z komory. Po vysu┼íen├¡
(vyt─øk├ín├¡) mobiln├¡ f├íze se provede detekce.
Ve v─øt┼íin─ø p┼Ö├¡pad┼» je mechanismem separace v pap├¡rov├®
chromatografii rozd─ølov├ín├¡ mezi dv─ø f├íze. Pap├¡r je nosi─ìem stacion├írn├¡ f├íze
(voda, resp. komplex celulóza-voda), po impregnaci mohou bÛt na papíře
zakotvena i jin├í rozpou┼ít─ødla (nap┼Ö. dimethylformamid, parafinov├¢ olej), ke
zvolen├® stacion├írn├¡ f├ízi se mus├¡ potom naj├¡t vhodn├í mobiln├¡ f├íze (zpravidla
sm─øs rozpou┼ít─ødel), kter├í zajist├¡, ┼¥e distribu─ìn├¡ konstanty hledan├¢ch slo┼¥ek se
od sebe budou li┼íit a dojde tedy k jejich rozd─ølen├¡.
RF: retarda─ìn├¡ faktor - je pom─ør vzd├ílenosti st┼Öedu skvrny od startu
(nanesení vzorku) ku vzdálenosti startu a čela (úroveň, kam došla mobilní
fáze).
ChromatografickÛ papír
ChromatografickÛ papír je čistÛ celulózovÛ papír
vyroben├¢ z tzv. lintersov├¢ch vl├íken (vyr├íb├¡ se z bavln─øn├¢ch zbytk┼»). Celul├│zov├¢
pap├¡r vykazuje silnou afinitu k vod─ø a je schopen sorbovat 5 - 20 %
hmotnostn├¡ch vody. Pro speci├íln├¡ ├║─ìely jsou dostupn├® modifikovan├® pap├¡ry -
nap┼Ö. pap├¡ry acetylovan├®, etherifikovan├® k d─ølen├¡ lipofiln├¡ch l├ítek, pap├¡ry
upraven├® pro iontovou v├¢m─ønu (IEC) s vysok├¢m obsahem voln├¢ch karboxylov├¢ch nebo
bazickÛch skupin.
Vyvíjecí komory
|
|
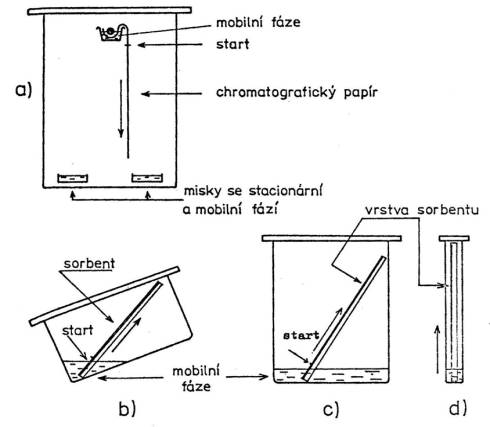
Pro vyv├¡jen├¡ pap├¡rov├¢ch chromatogram┼» se osv─ød─ìily komory
pro sestupn├® vyv├¡jen├¡ (a), v nich┼¥ se v horn├¡ ─ì├ísti um├¡st├¡ ┼¥l├íbek s mobiln├¡
f├íz├¡. Pro vzestupn├® vyv├¡jen├¡ (b, c, d) lze pou┼¥├¡t jakoukoli
n├ídobu s dob┼Öe t─øsn├¡c├¡m v├¡kem. Mobiln├¡ f├íze se um├¡st├¡ na dn─ø n├ídoby a vzl├¡n├í
vzhůru. |
Volba rozpou┼ít─ødlov├®ho syst├®mu v pap├¡rov├®
chromatografii
1.
Soustavy
s vodou jako stacion├írn├¡ zakotvenou f├íz├¡. Mobiln├¡ f├ízi tvo┼Ö├¡ organick├®
rozpou┼ít─ødlo (ni┼¥┼í├¡ alkoholy) ve sm─øsi s vodou. I kdy┼¥ v rozd─ølovac├¡
chromatografii plat├¡ z├ísada, ┼¥e mobiln├¡ a stacion├írn├¡ f├íze maj├¡ b├¢t nem├¡siteln├®
(aby nedoch├ízelo k vym├¢v├ín├¡ stacion├írn├¡ f├íze), v tomto p┼Ö├¡pad─ø je voda tvo┼Ö├¡c├¡
stacion├írn├¡ f├ízi pevn─ø v├íz├ína na celul├│zu, m├í charakter gelu a nen├¡ vym├¢v├ína z
pap├¡ru mobiln├¡ f├íz├¡. Tento typ soustavy je vhodn├¢ pro d─ølen├¡ hydrofiln├¡ch
polárních látek neutrální povahy (např. cukry, sulfokyseliny). Sníŝení obsahu
vody v mobilní fázi vede ke sníŝení hodnoty RF, naopak zvÛšení
obsahu vody, nebo pou┼¥it├¡ organick├®ho rozpou┼ít─ødla o vy┼í┼í├¡ polarit─ø umo┼¥┼êuje
vy┼í┼í├¡ pohyblivost d─ølen├¢ch l├ítek a vede ke vzr┼»stu hodnot RF.
2.
Soustavy
s pol├írn├¡mi organick├¢mi rozpou┼ít─ødly jako stacion├írn├¡ f├íz├¡. Chromatografick├¢
pap├¡r se naimpregnuje zvolenou stacion├írn├¡ f├íz├¡, po vyt─øk├ín├¡ rozpou┼ít─ødla, v
n─øm┼¥ byla stacion├írn├¡ f├íze rozpu┼ít─øna, se nan├í┼í├¡ vzorky na start. Takto
zakotveny bÛvají jako stacionární fáze formamid, dimethylformamid,
ethylenglykolmonoacetát aj. Mobilní fáze musí splňovat podmínku nerozpustnosti
s f├íz├¡ stacion├írn├¡, nej─ìast─øji se u┼¥├¡vaj├¡ sm─øsi uhlovod├¡k┼» - hexan, cyklohexan,
benzen, toluen, chloroform a další. Se stoupající polaritou mobilní fáze se
hodnoty RF zvyšují.
3.
Soustavy
s nepol├írn├¡mi organick├¢mi stacion├írn├¡mi f├ízemi (jsou rovn─ø┼¥ naz├¢v├íny soustavami
s obr├ícenou f├íz├¡). Jedn├í se o zakotven├¡ nepol├írn├¡ho rozpou┼ít─ødla (parafinov├¢
olej, silikonov├® oleje, laurylalkohol, 1-bromnaftalen apod.). Mobiln├¡ f├íz├¡
b├¢vaj├¡ sm─øsi pol├írn├¡ch organick├¢ch rozpou┼ít─ødel a vody (methanol, ethanol,
aceton, acetonitril, kyselina octová, formamid, dimethylformamid). Přídavek
organick├®ho rozpou┼ít─ødla v mobiln├¡ f├ízi v┼¥dy zvy┼íuje RF stejn─ø tak
jako sn├¡┼¥en├¡ koncentrace impregna─ìn├¡ho roztoku zakotven├® f├íze. Pojem obr├ícen├®
f├íze je odvozen z toho, ┼¥e po┼Öad├¡ separovan├¢ch slo┼¥ek se v tomto syst├®mu
obrac├¡, nejmen┼í├¡ hodnoty RF maj├¡ ty l├ítky, kter├® jsou nejm├®n─ø
pol├írn├¡ (hydrofobn├¡ s del┼í├¡mi alkylov├¢mi ┼Öet─øzci) a jsou tedy v├¡ce rozpustn├® ve
stacionární (nepolární, hydrofobní) fázi.
Detekce v pap├¡rov├® a tenkovrstv├® chromatografii
V plo┼ín├®m uspo┼Ö├íd├ín├¡ chromatografie je t┼Öeba odhalit
m├¡sta na chromatogramu, kde se vyskytuj├¡ rozd─ølen├® slo┼¥ky v├¢choz├¡ sm─øsi.
1.
Fyzikální
způsoby detekce spočívají ve vyuŝití záření -
viditeln├®ho, ultrafialov├®ho nebo infra─ìerven├®ho dopadaj├¡c├¡ho na chromatogram.
N─økter├® l├ítky se projevuj├¡ jako fluoreskuj├¡c├¡ skvrny, jin├® naopak UV sv─øtlo
zh├í┼íej├¡ a projev├¡ se jako tmav├® skvrny na sv├¡t├¡c├¡m pozad├¡ (tenk├í vrstva je v
tomto p┼Ö├¡pad─ø impregnov├ína nap┼Ö. fluorescen─ìn├¡m indik├ítorem).
2.
Chemick├®
způsoby detekce spočívají v tom, ŝe se chromatogram postříká vhodnÛm detekčním
─ìinidlem, kter├® vyvol├í barevnou reakci s rozd─ølen├¢mi l├ítkami. Pro detekci na
tenkÛch vrstvách se pouŝívá řady univerzálních detekčních činidel, zpravidla
agresívních chemikálií (kyselina dusičná, kyselina sírová, roztok dichromanu
sodn├®ho, manganistanu draseln├®ho apod.). Selektivn├¡ zp┼»soby detekce umo┼¥┼êuj├¡
detegovat ur─ìitou skupinu l├ítek, nap┼Ö. acidobazick├® indik├ítory rozli┼í├¡ na
chromatogramu kyseliny a báze, Ehrlichovo činidlo (2-dimethylaminobenzaldehyd)
reaguje pouze s aminy, ninhydrin a izatin reaguje s aminokyselinami a n─økter├¢mi
aminy atd. Ke zv├¢┼íen├¡ citlivosti detekce a mnohdy i k umo┼¥n─øn├¡ detekce v┼»bec se
často provádí derivatizace.
3.
Ostatní
způsoby detekce vyuŝívají různÛch vlastností separovanÛch látek - např. vyuŝití
biologickÛch vlastností látky (růst mikroorganismů).
Hodnocen├¡ chromatogramu v pap├¡rov├® a tenkovrstv├®
chromatografii
Kvalitativní hodnocení
P┼Öi potvrzov├ín├¡ identity analyzovan├® l├ítky s l├ítkou ji┼¥
známou se vychází ze skutečnosti, ŝe pro kaŝdou sloučeninu je za danÛch
podmínek charakteristická její poloha na chromatogramu (RF) a
chování při detekci (zbarvení, fluorescence apod.).
Kvantitativní hodnocení
Při kvantitativním vyhodnocování se uplatňují jak
postupy p┼Ö├¡m├® (in situ), tak postupy nep┼Ö├¡m├®. Nep┼Ö├¡m├¢ postup spo─ì├¡v├í v extrakci
l├ítky z vrstvy a n├ísledn├®m stanoven├¡ spektrofotometricky v UV, VIS, I─î,
p┼Ö├¡padn─ø fluorimetricky, nebo nejsou-li eluovan├® l├ítky barevn├®, fotometruj├¡ se
po reakci s barvotvorn├¢m ─ìinidlem. P┼Ö├¡m├® hodnocen├¡ slo┼¥ek na tenk├® vrstv─ø se
b─ø┼¥n─ø prov├íd├¡ denzitometrick├¢m m─ø┼Öen├¡m hustoty a plochy skvrny nebo p┼Ö├¡mou
fluorimetrií skvrn na desce. Pro kvantitativní hodnocení je základní podmínkou
reprodukovateln├® nan├í┼íen├¡ p┼Öesn├®ho objemu vzork┼».
Autorsk├® pozn├ímky
Jaroslava Vávrová