Abstrakt
Cystein pat┼Ö├Ł mezi semiesenci├Īln├Ł glukoplastick├®
aminokyseliny. Cystein je zdroj v┼Īech slou─Źenin s├Łry v organismu, ├║─Źastn├Ł
se ┼Öady biochemick├Įch enzymatick├Įch reakc├Ł. Disulfidov├® vazby, kter├® je schopen
cystein tvo┼Öit, hraj├Ł d┼»le┼Šitou roli p┼Öi formov├Īn├Ł prostorov├® struktury
b├Łlkovin a jejich fixaci.
Terminologie
Cystein, 2-amino-3-merkaptopropion├Īt
Synonyma
2-amino-3-merkaptopropion├Īt
Odkazy na jin├®
relevantn├Ł dokumenty, dal┼Ī├Ł informace
Chemick├Ī a fyzik├Īln├Ł
charakteristika, struktura a povaha analytu
Cystein (Cys), NH2CH(CH2SH)COOH,
C3H7O2SN
m.h. 121,2
Kysel├Ī disocia─Źn├Ł konstanta pK (25 oC)
1,71; 8,33 (SH); 10,78
Izoelektrick├Į bod pI 5,02
Cystein je semiesenci├Īln├Ł aminokyselina, tzv.
ŌĆØpodm├Łn─øn─ø postradateln├ĪŌĆØ pouze p┼Öi dostatku esenci├Īln├Ł aminokyseliny ŌĆō methioninu.
Podle chemick├®ho charakteru postrann├Łho ┼Öet─øzce ┼Öad├Łme cystein mezi pol├Īrn├Ł
aminokyseliny. Pol├Īrn├Ł funk─Źn├Ł skupina cysteinu vytv├Ī┼Ö├Ł snadno pol├Īrn├Ł
interakce, zejm├®na vod├Łkov├® vazby. Thiolov├Ī skupina p┼Öisp├Łv├Ī k hydrofiln├Łm
vlastnostem b├Łlkoviny, je snadno oxidovateln├Ī a umo┼Š┼łuje vytv├Ī┼Öen├Ł
disulfidov├Įch vazeb (vznik cystinu). Tyto vazby hraj├Ł d┼»le┼Šitou roli ve struktu┼Öe
b├Łlkovin ŌĆō p┼Öi formov├Īn├Ł prostorov├® struktury a jej├Ł fixaci. Z├Īrove┼ł dod├Īvaj├Ł
┼Öet─øzc┼»m vhodn├® mechanick├® vlastnosti (nap┼Ö. pru┼Šnost v elastick├Įch
─Ź├Īst├Łch pojiva) a ovliv┼łuj├Ł tak├® chemick├® vlastnosti peptid┼» a b├Łlkovin.
Cystein obsahuje asymetrick├Į atom uhl├Łku, existuje
proto ve dvou enantiomern├Łch konfigurac├Łch ŌĆō D a L, v b├Łlkovin├Īch se
vyskytuj├Ł pouze L-formy.
Role v metabolismu
Atom s├Łry je jeden z nejlep┼Ī├Łch nukleofil┼»,
proto se cystein ├║─Źastn├Ł ┼Öady biochemick├Įch enzymatick├Įch reakc├Ł. Cystein je
prekurzorem koenzymu A a sou─Ź├Īst├Ł tripeptidu ŌĆō glutathionu.
Glutathion m├Ī r┼»zn├® funkce ŌĆō je kofaktor enzym┼»,
├║─Źastn├Ł se detoxikace voln├Įch radik├Īl┼», tvo┼Ö├Ł rezervu thiolov├Įch skupin.
Keratin obsahuje asi 14% cysteinu, ten tvo┼Ö├Ł
p┼Ö├Ł─Źn├® s├Ł┼źov├Īn├Ł disulfidov├Įmi vazbami, kter├® zaru─Źuj├Ł vysokou pevnost (keratin
je z├Īkladem rohoviny).
Zdroj (synt├®za,
p┼Ö├Łjem)
Cystein pat┼Ö├Ł mezi semiesenci├Īln├Ł aminokyseliny, tvo┼Ö├Ł se
z esenci├Īln├Łho metioninu. Methionin je p┼Öem─øn─øn na homocystein (50%
dostupn├®ho homocysteinu je recyklov├Īno zp─øt na methionin). Homocystein m┼»┼Še b├Įt
tak├® slou─Źen se serinem a vytvo┼Öit cystathionin (za p┼Ö├Łtomnosti
pyridoxalfosf├Ītu). Cystathionin
je deaminov├Īn a ┼Īt─øpen na cystein a 2-oxobutyr├Īt.
Pr┼»myslov─ø je cystein (stejn─ø jako v─øt┼Īina
aminokyselin) vyr├Īb─øn biosynt├®zou u┼Šit├Łm mikroorganism┼» nebo chemickou synt├®zou
nebo kombinac├Ł chemick├® synt├®zy a r┼»zn├Įch biotechnologick├Įch postup┼». Je
pou┼Š├Łv├Īn jako sou─Ź├Īst├Ł krmiv pro u┼Šitkov├Ī zv├Ł┼Öata, ochucovadlo potravin,
konzerva─Źn├Ł a antioxida─Źn├Ł p┼Ö├Łpravky.
Distribuce v
organismu, obsah ve tk├Īn├Łch
V organismu je
cystein p┼Ö├Łtomen v plazm─ø i v mo─Źi, rychle se oxiduje na disulfid-cystin. Je
sou─Ź├Īst├Ł cel├® ┼Öady dal┼Ī├Łch sulfid┼» v mo─Źi p┼Ö├Łtomn├Įch jako nap┼Ö.:
S-methylcystein, S-karboxymethylcystein, Lcysteinylglycin. S-sulfo-L-cystein je
v├Įrazn─ø zv├Į┼Īen v mo─Źi u deficitu sulfitoxid├Īzy. Patologicky sn├Ł┼Šen├® hladiny v
krvi jsou zaznamen├Īny u ┼Öady d─ødi─Źn├Įch poruch metabolismu sirn├Įch aminokyselin,
jako nap┼Ö. u homocystinurie, deficitu methioninadenozyltransfer├Īzy.
Poruchy metabolismu sirn├Įch AMK.
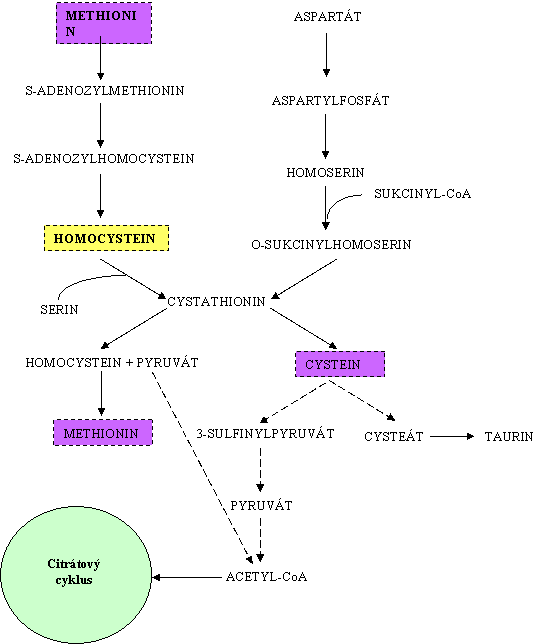
Zp┼»sob vylu─Źov├Īn├Ł nebo
metabolismusOSN-E
Cystein pat┼Ö├Ł mezi glukoplastick├® aminokyseliny.
Hlavn├Ł cesta odbour├Īv├Īn├Ł cysteinu je p┼Ö├Łmo na sulf├Īt a pyruv├Īt, pyruv├Īt je oxida─Źn├Ł dekarboxylac├Ł
p┼Öem─øn─øn na acetylkoenzym A (acetylCoA). AcetylCoA vstupuje do citr├Ītov├®ho cyklu
jako kone─Źn├Į produkt odbour├Īv├Īn├Ł cysteinu.
Vedlej┼Ī├Łm produktem odbour├Īv├Īn├Ł cysteinu je taurin.
Literatura
Z.Vodr├Ī┼Ška: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie.
Academia, Praha 1987.
Autorsk├® pozn├Īmky
Karol├Łna Pe┼Īkov├Ī
recenze Viktor Ko┼Šich