Abstrakt
Cystein patří mezi neesenciální glukoplastické
aminokyseliny. Cystein je zdroj všech sloučenin síry v organismu, účastní
se řady biochemických enzymatických reakcí. Disulfidové vazby, které je schopen
cystein tvořit, hrají důležitou roli při formování prostorové struktury
bílkovin a jejich fixaci.
Terminologie
Cystein, 2-amino-3-merkaptopropionát
Synonyma
2-amino-3-merkaptopropionát
Odkazy na jiné relevantní
dokumenty, další informace
Chemická a fyzikální
charakteristika, struktura a povaha analytu
Cystein (Cys), NH2CH(CH2SH)COOH, C3H7O2SN
m.h. 121,2
Kyselá disociační konstanta pK (25 oC)
1,71; 8,33 (SH); 10,78
Izoelektrický bod pI 5,02
Cystein je neesenciální aminokyselina, tzv. ”podmíněně
postradatelná” pouze při dostatku esenciální aminokyseliny – methioninu. Podle chemického
charakteru postranního řetězce řadíme cystein mezi polární aminokyseliny.
Polární funkční skupina cysteinu vytváří snadno polární interakce, zejména
vodíkové vazby. Thiolová skupina přispívá k hydrofilním vlastnostem
bílkoviny, je snadno oxidovatelná a umožňuje vytváření disulfidových vazeb
(vznik cystinu).
Tyto vazby hrají důležitou roli ve struktuře bílkovin – při formování
prostorové struktury a její fixaci. Zároveň dodávají řetězcům vhodné mechanické
vlastnosti (např. pružnost v elastických částích pojiva) a ovlivňují také
chemické vlastnosti peptidů a bílkovin.
Cystein obsahuje asymetrický atom uhlíku, existuje proto
ve dvou enantiomerních konfiguracích – D a L, v bílkovinách se vyskytují
pouze L-formy.
Role v metabolismu
Atom síry je jeden z nejlepších nukleofilů, proto
se cystein účastní řady biochemických enzymatických reakcí. Cystein je
prekurzorem koenzymu A a součástí tripeptidu – glutathionu.
Glutathion má různé funkce – je kofaktor enzymů, účastní
se detoxikace volných radikálů, tvoří rezervu thiolových skupin.
Keratin obsahuje asi 14% cysteinu, ten tvoří příčné
síťování disulfidovými vazbami, které zaručují vysokou pevnost (keratin je
základem rohoviny).
Zdroj (syntéza, příjem)
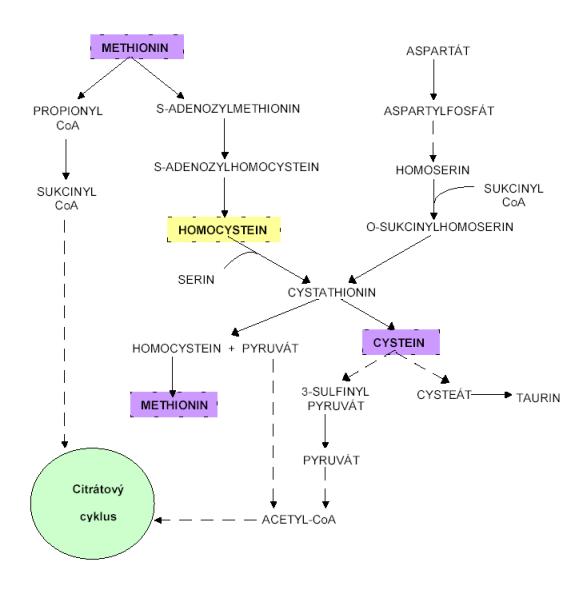
Cystein patří mezi neesenciální aminokyseliny, tvoří se
z esenciálního methioninu. V postranním řetězci serinu dochází k nahrazení
atomu kyslíku za atom síry, jeho zdrojem je methionin. Methionin je
syntetizován z aspartátu, meziprodukt této syntézy se kondenzuje se
serinem a vzniká cystathionin. Cystathionin je deaminován a štěpen na cystein a
2-oxobutyrát.
Průmyslově je cystein (stejně jako většina aminokyselin)
vyráběn biosyntézou užitím mikroorganismů nebo chemickou syntézou nebo
kombinací chemické syntézy a různých biotechnologických postupů. Je používán
jako součástí krmiv pro užitková zvířata, ochucovadlo potravin, konzervační a
antioxidační přípravky.
Distribuce v organismu, obsah
ve tkáních
V organismu je cystein přítomen v plazmě i v moči, rychle se oxiduje
na disulfid-cystin. Je součástí celé řady dalších sulfidů v moči přítomných
jako např.: S-methylcystein, S-karboxymethylcystein, L-cysteinylglycin.
L-cystinglycin a S-sulfo-L-cystein jsou výrazně zvýšeny
v moči u deficitu sulfitoxidázy.
Poruchy metabolismu sirných AMK.
Způsob vylučování nebo
metabolismus
Cystein patří mezi glukoplastické aminokyseliny. Hlavní cesta
odbourávání cysteinu je přímo na sulfát a pyruvát, pyruvát je oxidační dekarboxylací
přeměněn na acetylkoenzym A (acetylCoA). AcetylCoA vstupuje do citrátového cyklu
jako konečný produkt odbourávání cysteinu.
Vedlejším produktem odbourávání cysteinu je taurin.
Literatura
Z.Vodrážka: Biochemie. Academia, Praha 1992.
P.Karlson, W.Gerok, W.Gross: Pathobiochemie. Academia,
Praha 1987.
Autorské poznámky
Karolína Pešková
recenze Josef Hyánek